3. Лечение, включая медикаментозную и немедикаментозную терапии
3.1 Медикаментозная терапия
3.1.1 Лечение стабильной астмы
3.1.1.1 Генно-инженерные биологические препараты (ГИБП) из фармакологической группы R03DX
Рис. 1 Ступенчатая терапия БА для подростков с 12 лет и взрослых
Рис. 2 Ступенчатая терапия БА для детей от 6 до 11 лет
Рис. 3 Ступенчатая терапия БА для детей до 5 лет
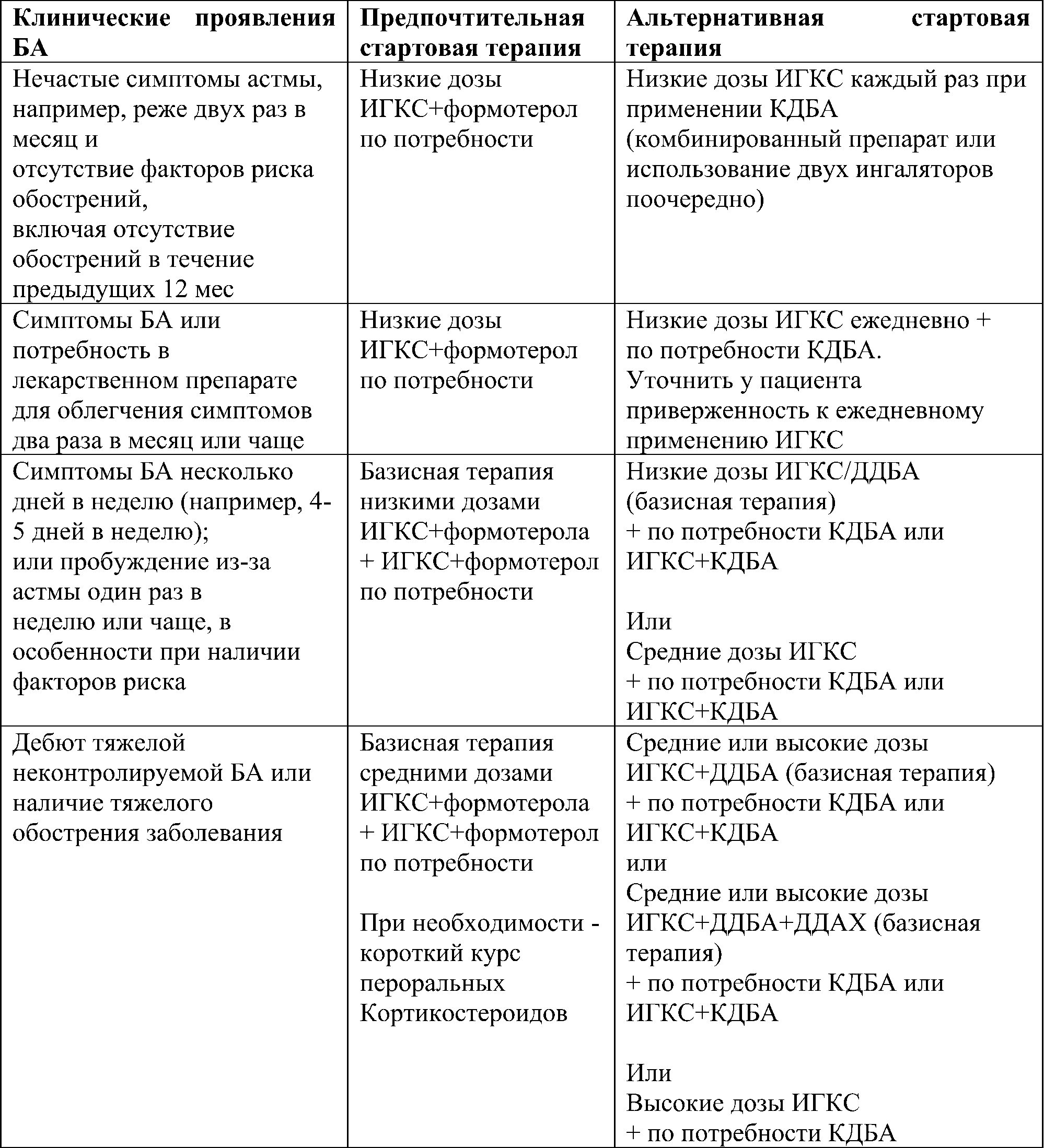
Таблица 7. Стартовая терапия БА (взрослые и дети старше 12 лет)
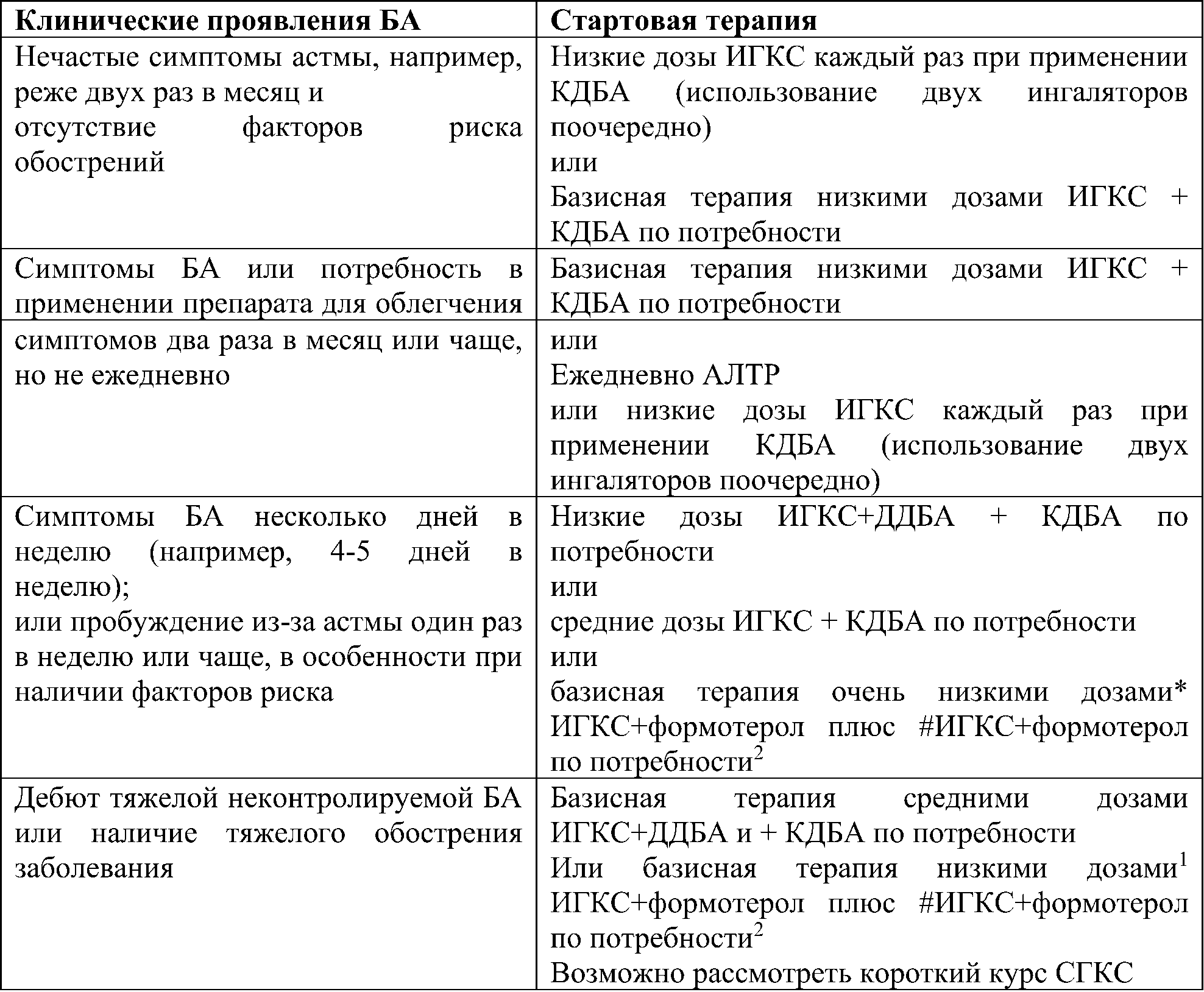
Таблица 8. Стартовая терапия БА (дети от 6 до 11 лет)
3.1 Медикаментозная терапия
3.1.1 Лечение стабильной астмы
3.1.1.1 Генно-инженерные биологические препараты (ГИБП) из фармакологической группы R03DX
Рис. 1 Ступенчатая терапия БА для подростков с 12 лет и взрослых
Рис. 2 Ступенчатая терапия БА для детей от 6 до 11 лет
Рис. 3 Ступенчатая терапия БА для детей до 5 лет
Таблица 7. Стартовая терапия БА (взрослые и дети старше 12 лет)
Таблица 8. Стартовая терапия БА (дети от 6 до 11 лет)
3. Лечение, включая медикаментозную и немедикаментозную терапии,
диетотерапия, обезболивание, медицинские показания и противопоказания к применению методов лечения.
Основной целью современной терапии БА является:
достижение и поддержание контроля над симптомами БА в течение длительного времени и минимизация рисков будущих обострений БА, фиксированной обструкции и нежелательных побочных эффектов от проводимой терапии.
достижение и поддержание контроля над симптомами БА в течение длительного времени и минимизация рисков будущих обострений БА, фиксированной обструкции и нежелательных побочных эффектов от проводимой терапии.
При лечении БА рекомендуется использовать ступенчатый подход, корректируя объем терапии в зависимости от уровня контроля и наличия факторов риска обострений БА (Рис. 1-3, Табл. 7-8).
Каждая ступень включает варианты терапии, которые могут служить альтернативами при выборе поддерживающей терапии БА, хотя и не являются одинаковыми по эффективности (Рис. 1-3). Первоначальный выбор ступени терапии зависит от выраженности клинических проявлений БА и наличия факторов риска обострений заболевания (Табл 7-8).
Предлагается на выбор две схемы выбора препаратов для контролирующей (базисной) и симптоматической (для купирования симптомов) терапии.
Первая схема является предпочтительной (Рис.1-3)
Первая схема является предпочтительной (Рис.1-3)
Увеличение объема терапии (шаг вверх согласно ступенчатому подходу к лечению) следует проводить, если БА остается неконтролируемой, несмотря на хорошую приверженность к лечению и правильную технику использования ингалятора.
Прежде чем пересмотреть объем лечения необходимо убедиться, что пациент выполняет все рекомендации, не допускает ошибок при использовании устройства доставки лекарственного средства, симптомы пациента вызваны именно БА, отсутствует воздействие причинно-значимого аллергена и фактор мультиморбидности.
Прежде чем пересмотреть объем лечения необходимо убедиться, что пациент выполняет все рекомендации, не допускает ошибок при использовании устройства доставки лекарственного средства, симптомы пациента вызваны именно БА, отсутствует воздействие причинно-значимого аллергена и фактор мультиморбидности.
Снижение объема терапии показано при достижении и сохранении стабильного контроля ≥ 3 месяцев и отсутствии факторов риска с целью установления минимального объема терапии и наименьших доз препаратов, достаточных для поддержания контроля.
При принятии решения, какой препарат снижать первым и с какой скоростью, рекомендуется принять во внимание тяжесть БА, побочные эффекты лечения, продолжительность приема текущей дозы, достигнутый положительный эффект и предпочтения пациента.
Снижение дозы ИГКС должно быть медленным в связи с возможностью развития обострения.
При достаточном контроле возможно снижение дозы каждые три месяца, примерно на 25-50%.
При принятии решения, какой препарат снижать первым и с какой скоростью, рекомендуется принять во внимание тяжесть БА, побочные эффекты лечения, продолжительность приема текущей дозы, достигнутый положительный эффект и предпочтения пациента.
Снижение дозы ИГКС должно быть медленным в связи с возможностью развития обострения.
При достаточном контроле возможно снижение дозы каждые три месяца, примерно на 25-50%.
К факторам риска обострений после уменьшения объема терапии относят наличие обострений в анамнезе и/или госпитализаций по поводу обострения БА в течение предыдущих 12 месяцев, низкий исходный уровень ОФВ1.
Бронхиальная гиперреактивность и эозинофилия в мокроте так же являются предикторами возможной потери контроля над БА при снижении дозы поддерживающего лечения.
Бронхиальная гиперреактивность и эозинофилия в мокроте так же являются предикторами возможной потери контроля над БА при снижении дозы поддерживающего лечения.
План действий по уменьшению объема терапии — снижению ступени лечения, у взрослых и подростков с хорошо контролируемой астмой представлен в Приложении Б16.
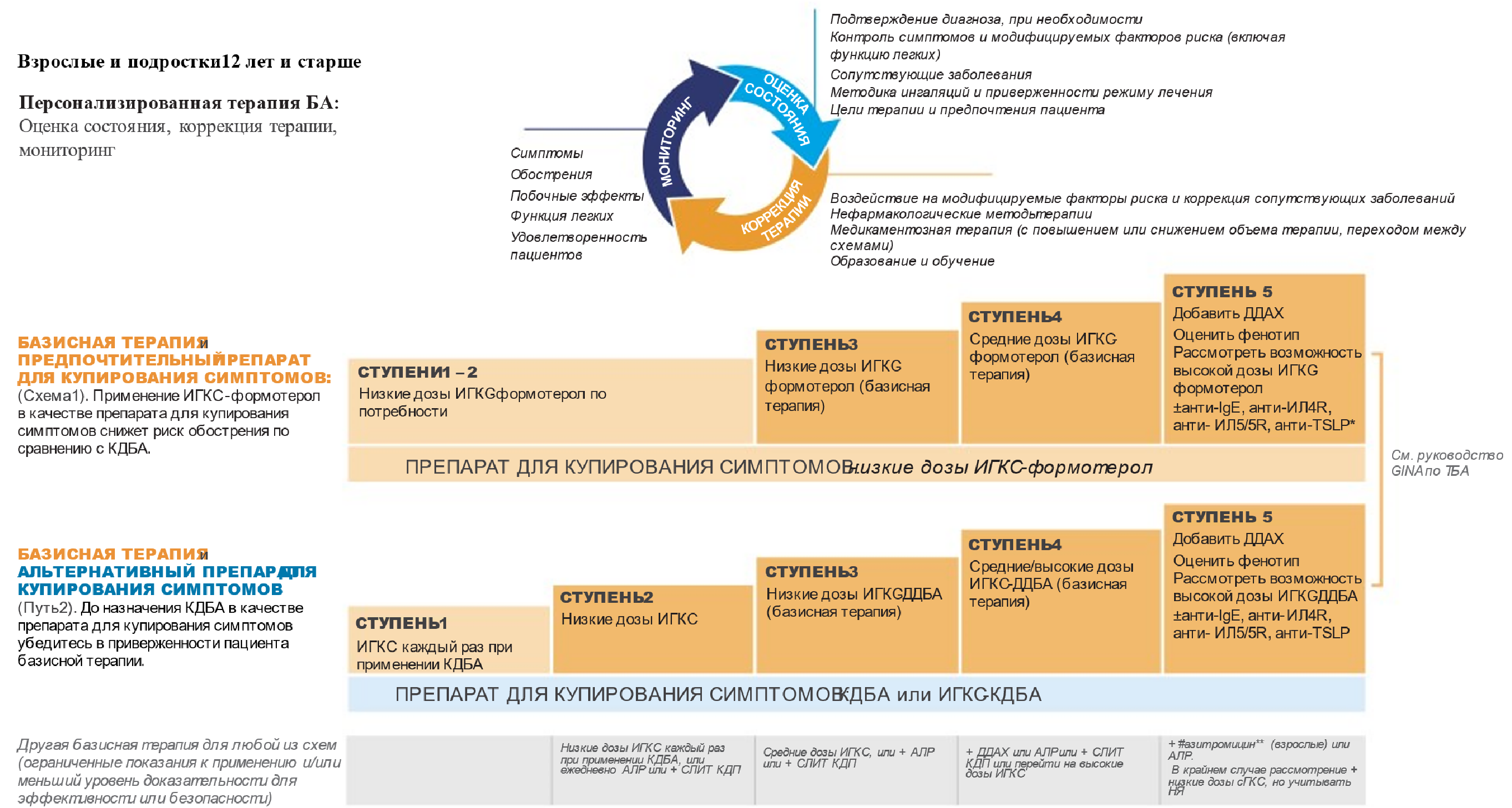
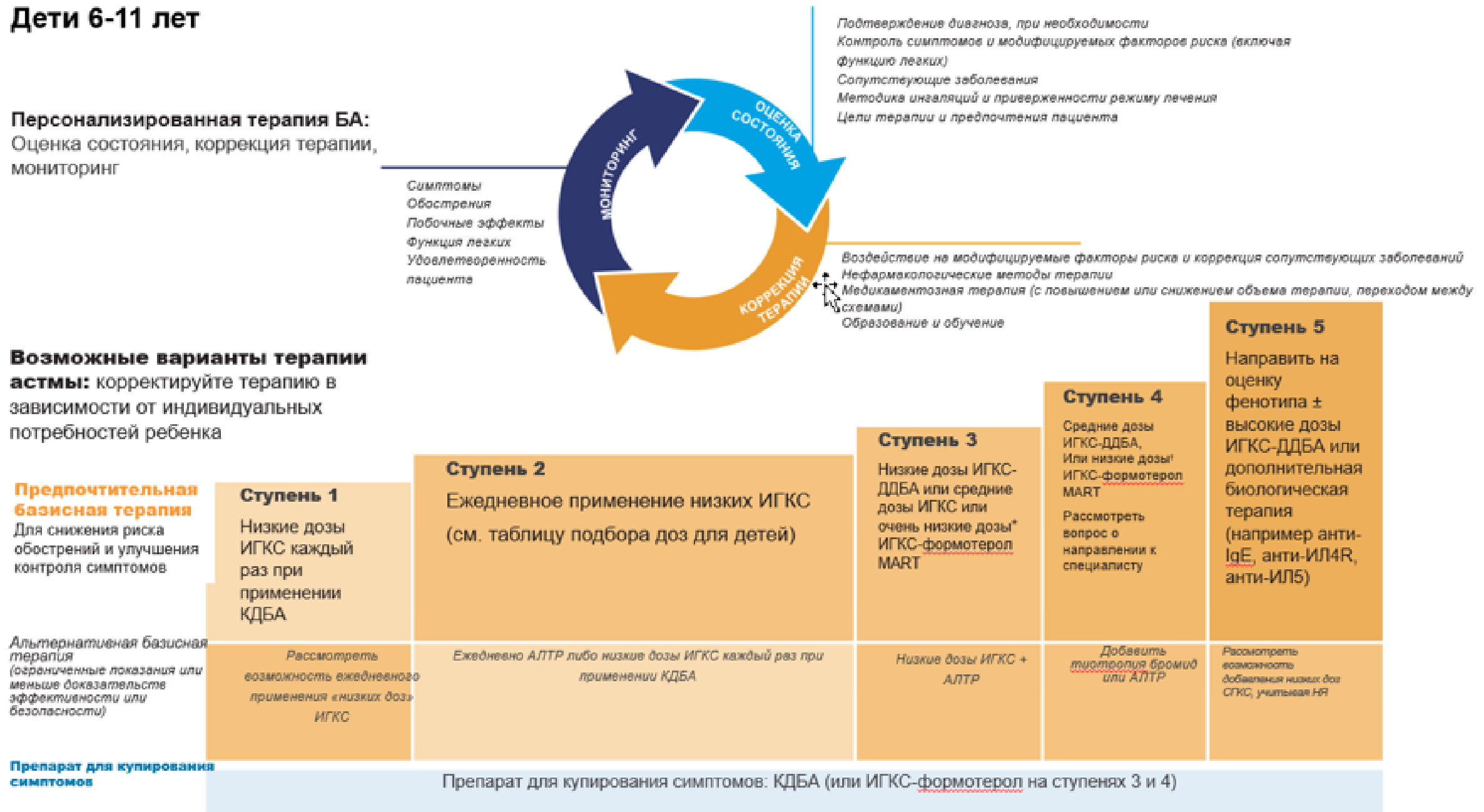
Примечание: ИГКС – ингаляционные глкюкортикостероиды, КДБА – коротко действующие β2-агонисты, ДДБА — длительно действующие β2-агонисты
ДДАХ – длительно действующие антихолинергические средства, АЛТР – антагонисты лейкотриеновых рецепторов; ИГКС – ингаляционные глюкокортикостероиды – (код по АТХ R01AD),
сГКС – системные глюкокортикостероиды, СИТ – аллерген-специфическая иммунотерапия, КДП – клещ домашней пыли. Очень низкие дозы: БУД-ФОРМ 100/6 мкг
сГКС – системные глюкокортикостероиды, СИТ – аллерген-специфическая иммунотерапия, КДП – клещ домашней пыли. Очень низкие дозы: БУД-ФОРМ 100/6 мкг
† Низкие дозы: БУД-ФОРМ 200/6 мкг (отмеренные дозы).
*В настоящее время у детей 6-11 лет препарат Симбикорт® не зарегистрирован для комбинированной терапии в режиме одного ингалятора терапии легкой бронхиальной астмы и для купирования симптомов
Примечание: ИГКС – ингаляционные глюкортикостероиды, КДБА – коротко действующие β2-агонисты, ДДБА — длительно действующие β2 ДДАХ – длительно действующие антихолинергические средства, АЛТР – антагонисты лейкотриеновых рецепторов; ИГКС глюкокортикостероиды – (код по АТХ R01AD).
агонисты – ингаляционные
1 Таблицы с низкими, средними и высокими дозами ИГКС для детей, подростков и взрослых в Приложении А3.2, А3.3.
2 В РФ режим единого ингалятора одобрен для детей с 12 лет
Детям младше 5 лет рекомендуется в качестве стартовой терапии выбрать низкие дозы ИГКС (Приложение А3.4) в сочетании с препаратами по требованию (КДБА) для облегчения симптомов БА [21]. Низкие дозы ИГКС обеспечивают хороший клинический эффект у большинства детей, в то время как высокие — связаны с повышенным риском развития местных и системных побочных эффектов.
• Рекомендуется рассмотреть назначение комбинированного бронходилатирующего средства (селективного бета2-адреномиметика и глюкокортикостероида местного) будесонид + формотерол** (R03AK07) пациентам с легкой БА старше 12 лет или беклометазон + формотерол** (R03AK08) или сальбутамол + беклометазон (R03AK13) пациентам старше 18 лет в режиме применения по потребности для снятия симптомов и приступов удушья с целью реализации быстрого бронхолитического и противовоспалительного действия.
Уровень убедительности рекомендаций -А (уровень достоверности доказательств — 2)
Комментарии:
Данный режим терапии является предпочтительным для пациентов с легкой БА старше 12 лет (или старше 18 лет с учетом возрастных ограничений по определенным комбинациям) на 1-2 ступенях терапии.
Назначение низких доз ИГКС в качестве противовоспалительной терапии вместе с препаратом, облегчающим симптомы (формотерол или КДБА) значимо снижает риск тяжелых обострений заболевания в сравнении с монотерапией КДБА по потребности.
Помимо применения для снятия симптомов возможно предупредительное применение перед физической нагрузкой или планируемым контактом с причинно-значимыми аллергенами.
Комментарии:
Данный режим терапии является предпочтительным для пациентов с легкой БА старше 12 лет (или старше 18 лет с учетом возрастных ограничений по определенным комбинациям) на 1-2 ступенях терапии.
Назначение низких доз ИГКС в качестве противовоспалительной терапии вместе с препаратом, облегчающим симптомы (формотерол или КДБА) значимо снижает риск тяжелых обострений заболевания в сравнении с монотерапией КДБА по потребности.
Помимо применения для снятия симптомов возможно предупредительное применение перед физической нагрузкой или планируемым контактом с причинно-значимыми аллергенами.
Будесонид + формотерол** (код АТХ: R03AK07) в дозированном порошковом ингаляторе взрослым и подросткам от 12 лет 160/4,5 мкг по 1-2 инг по потребности (желательно не превышать 6 инг в сут, максимальная доза по потребности 12 инг/сут).
Следует обращать внимание, что не все ингаляторы, зарегистрированные на территории РФ и содержащие данную фиксированную комбинацию, имеют в инструкции указание на возможность применения в режиме по потребности.
Следует обращать внимание, что не все ингаляторы, зарегистрированные на территории РФ и содержащие данную фиксированную комбинацию, имеют в инструкции указание на возможность применения в режиме по потребности.
Беклометазон + формотерол** (код АТХ: RO3AKO8) в дозированном аэрозольном ингаляторе взрослым (от 18 лет) 100/6 мкг по 1-2 инг по потребности (максимальная доза по потребности 6 инг/сут).
Беклометазон + сальбутамол (код АТХ: RO3AK13 ) в дозированном аэрозольном ингаляторе взрослым (от 18 лет) 250/100 мкг по 1-2 инг по потребности (максимальная доза по потребности 8 инг/сут).
• Рекомендуется рассмотреть назначение селективного бета2-адреномиметика (КДБА) совместно с низкими дозами глюкокортикостероида местного (ИГКС) последовательно из двух отдельных ингаляторов пациентам с легкой БА от 6 до 11 лет и в качестве альтернативной терапии пациентам старше 12 лет по потребности для снятия симптомов и приступов удушья с целью реализации быстрого бронхолитического и противовоспалительного действия.
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: на 1-2 ступенях монотерапия КДБА в режиме по потребности при легкой БА более не рекомендуется.
Чрезмерное использование КДБА является небезопасным: выдача ≥3 ингаляторов КДБА в год увеличивает риск обострений БА, применение ≥12 ингаляторов КДБА в год связано с повышенным риском смерти по причине БА.
Комментарии: на 1-2 ступенях монотерапия КДБА в режиме по потребности при легкой БА более не рекомендуется.
Чрезмерное использование КДБА является небезопасным: выдача ≥3 ингаляторов КДБА в год увеличивает риск обострений БА, применение ≥12 ингаляторов КДБА в год связано с повышенным риском смерти по причине БА.
Для детей возможно использование ДАИ через спейсер или применение препаратов через небулайзер.
I) В качестве бета2-адреномиметика селективного возможно, например:
Сальбутамол** (код АТХ: RO3ACO2 ) в дозированном аэрозольном ингаляторе детям с 2 лет и взрослым 100-200 мкг по потребности (максимальная доза 800 мкг/сут), в виде раствора для ингаляций с возраста 18 мес. по 2,5-5 мг на ингаляцию (максимальная суточная доза 20 мг);
Сальбутамол** (код АТХ: RO3ACO2 ) в дозированном аэрозольном ингаляторе детям с 2 лет и взрослым 100-200 мкг по потребности (максимальная доза 800 мкг/сут), в виде раствора для ингаляций с возраста 18 мес. по 2,5-5 мг на ингаляцию (максимальная суточная доза 20 мг);
Фенотерол (код АТХ: RO3ACO4) в дозированном аэрозольном ингаляторе взрослым (от 18 лет) 100-200 мкг по 1-2 инг по потребности (максимальная доза по потребности 8 инг/сут);
Левосальбутамол (код АТХ: R03AC) в дозированном аэрозольном ингаляторе детям от 4 лет и взрослым 45-90 мкг по потребности (максимальная доза 540 мкг/сут);
или комбинированный препарат: Ипратропия бромид + фенотерол** (код АТХ: R03AL01) р-р для ингаляций 0.25 мг+0.5 мг/мл с помощью небулайзера или ДАИ 20 мкг + 50 мкг со спейсером (согласно Инструкции).
II) В качестве глюкокортикостероида местного возможно, например:
Флутиказон (код АТХ: R03BA05) в дозированном аэрозольном ингаляторе детям от 6 лет 50-125 мкг и взрослым 125-250 мкг после ингаляции КДБА.
Флутиказон (код АТХ: R03BA05) в дозированном аэрозольном ингаляторе детям от 6 лет 50-125 мкг и взрослым 125-250 мкг после ингаляции КДБА.
Будесонид** (код АТХ: R03BA02) в дозированном порошковом ингаляторе детям от 6 лет и взрослым 100-200 мкг или в виде виде суспензии для ингаляций детям от 6 мес (дозировки согласно Инструкции) и взрослым с помощью небулайзера или р-ра для ингаляций детям с 16 лет и взрослым с помощью небулайзера 250 мкг после ингаляции КДБА.
52
Беклометазон** (код АТХ: R03BA01) в дозированном аэрозольном ингаляторе детям от 6 лет и взрослым 100-200 мкг после ингаляции КДБА.
Циклесонид (код АТХ: R03BA08) в дозированном порошковом ингаляторе детям от 12 лет и взрослым 160 мкг после ингаляции КДБА.
• Рекомендуется рассмотреть возможность назначения глюкокортикостероида местного (ИГКС) в низкой дозе в ежедневном режиме с использованием бета-2-адреномиметика селективного (КДБА) по потребности детям в возрасте от 6 до 11 лет с легкой БА (симптомы не чаще 2 раз в месяц) и наличием факторов риска обострения в качестве альтернативного подхода к лечению [21,128,136142].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии:
следует учитывать вероятность низкой приверженности к лечению у детей с легкой БА при данном подходе (невыполнение рекомендаций о ежедневном применении ИГКС и, как следствие, риске использования КДБА без одновременного применения с ИГКС). Ниже приведены препараты и приблизительные дозы, которые могут быть рекомендованы к назначению на 2 ступени терапии. Подробнее о выборе доз ИГКС см. Приложение А3.2, А3.3.
Комментарии:
следует учитывать вероятность низкой приверженности к лечению у детей с легкой БА при данном подходе (невыполнение рекомендаций о ежедневном применении ИГКС и, как следствие, риске использования КДБА без одновременного применения с ИГКС). Ниже приведены препараты и приблизительные дозы, которые могут быть рекомендованы к назначению на 2 ступени терапии. Подробнее о выборе доз ИГКС см. Приложение А3.2, А3.3.
Например:
Флутиказон (код АТХ: R03BA05) в дозированном аэрозольном ингаляторе детям от 4 лет 50 мкг * 1-2 р в день.
Будесонид** (код АТХ: R03BA02) в дозированном порошковом ингаляторе детям от 6 лет 100 мкг * 1-2 р в день.
Будесонид** (код АТХ: R03BA02) в виде суспензии для ингаляций дозированной с помощью небулайзера детям от 6 мес (дозировки согласно Инструкции) или р-ра для ингаляций детям от 16 лет 250 мкг* 1-2 р в день
Беклометазон** (код АТХ: R03BA01) в дозированном аэрозольном ингаляторе детям от 4 до 12 лет 100 мкг * 1-2 р в день.
• Рекомендуется назначение селективного бета-2-адреномиметика (КДБА, код АТХ R03AC) или в сочетании с м-холиноблокатором (код АТХ R03AL) детям младше 5 лет с установленным диагнозом БА легкой степени тяжести (симптомы не чаще 2 раз в месяц) по потребности в случае нечастых эпизодов свистящего дыхания, в том числе на фоне респираторных инфекций, если в промежутках между эпизодами жалобы отсутствуют или носят единичный характер.
Уровень убедительности рекомендаций — B (уровень достоверности доказательств — 3)
Комментарии:
на 1 ступени терапии следует придерживаься стратегии назначения КДБА с ИГКС для исключения избыточного применения КДБА и неконтролируемого течения астмы.
Комментарии:
на 1 ступени терапии следует придерживаься стратегии назначения КДБА с ИГКС для исключения избыточного применения КДБА и неконтролируемого течения астмы.
Потребность в КДБА для облегчения симптомов более двух раз в неделю в течение 1 месяца указывает на необходимость пересмотра лечения и переходу к назначению низких доз ИГКС в качестве ежедневной противовоспалительной базисной терапии.
Для детей данной возрастной категории при выборе средства доставки следует руководствоваться доступностью, предпочтением родителей и возможностями пациента (в том числе для КДБА – спейсер либо небулайзер с маской или мундштуком).
Не рекомендовано детям младше 5 лет для купирования симптомов назначение адренергических средств системного действия (код по АТХ R03C) вследствие их отложенного действия и высокой частоты побочных эффектов по сравнению с ингаляционными КДБА.
Например, могут применяться:
Сальбутамол** (код АТХ: R03AC02) в виде раствора для ингаляций с возраста 18 мес. по 2,5-5 мг на ингаляцию (максимальная суточная доза 20 мг); в дозированном аэрозольном ингаляторе детям с 2 лет и взрослым, в среднем, 100 мкг по потребности (максимальная доза 800 мкг/сут);
Левосальбутамол (код АТХ: R03AC) в дозированном аэрозольном ингаляторе детям от 4 лет и взрослым 45-90 мкг по потребности (максимальная доза 540 мкг/сут);
или комбинированный препарат: Ипратропия бромид + фенотерол** (код АТХ: R03AL01) р-р для ингаляций 0.25 мг+0.5 мг/мл с помощью небулайзера или ДАИ 20 мкг + 50 мкг со спейсером (согласно Инструкции).
• Рекомендуется рассмотреть назначение комбинированного бронходилатирующего средства (бета2-адреномиметика селективного и глюкокортикостероида местного) будесонид + формотерол** (R03AK07) пациентам с легкой БА и наличием факторов риска обострения или среднетяжелой БА старше 12 лет или беклометазон + формотерол** (R03AK08) пациентам старше 18 лет для регулярной терапии астмы и применения по потребности для снятия симптомов и приступов удушья в режиме единого ингалятора.
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Комментарии:
на 3 ступени терапии указанный режим терапии позволит избежать типичного для пациентов с легкой астмой отказа от ИГКС, сохранив минимальный объем противовоспалительной терапии в период появления симптомов.
У взрослых и подростков комбинация ИГКС+формотерол в качестве комбинированной терапии в режиме единого ингалятора — как поддерживающей, так и облегчающей симптомы — более эффективна для снижения частоты обострений, по сравнению с теми же дозами ИГКС+ДДБА или более высокими дозами ИГКС базисной терапии.
Наилучший эффект при переходе на комбинированную терапию наблюдается у пациентов с тяжелыми обострениями в анамнезе
на 3 ступени терапии указанный режим терапии позволит избежать типичного для пациентов с легкой астмой отказа от ИГКС, сохранив минимальный объем противовоспалительной терапии в период появления симптомов.
У взрослых и подростков комбинация ИГКС+формотерол в качестве комбинированной терапии в режиме единого ингалятора — как поддерживающей, так и облегчающей симптомы — более эффективна для снижения частоты обострений, по сравнению с теми же дозами ИГКС+ДДБА или более высокими дозами ИГКС базисной терапии.
Наилучший эффект при переходе на комбинированную терапию наблюдается у пациентов с тяжелыми обострениями в анамнезе
Будесонид + формотерол** (код АТХ: RO3AKO7 ) в дозированном порошковом ингаляторе взрослым и подросткам от 12 лет 160/4,5 мкг по 1-2 инг * 2 р в день на регулярной основе и по 1-2 инг по потребности (желательно не превышать 6 инг в сут, максимальная доза по потребности 12 инг/сут). Следует обращать внимание, что не все ингаляторы, зарегистрированные на территории РФ и содержащие данную фиксированную комбинацию, имеют в инструкции указание на возможность применения в режиме по потребности и, соответственно, в режиме единого ингалятора.
Беклометазон + формотерол** (код АТХ: R03AR08) в дозированном
аэрозольном ингаляторе взрослым (от 18 лет) 100/6 мкг по 1-2 инг * 2 р в день на регулярной основе и по 1-2 инг по потребности (максимальная доза по потребности 6 инг/сут).
Беклометазон + сальбутамол (код АТХ: R03AK08) в дозированном аэрозольном ингаляторе взрослым (от 18 лет) 250/100 мкг по 2 инг * 2 р в день на регулярной основе и по 1-2 инг по потребности (максимальная доза по потребности 8 инг/сут).
• Рекомендуется рассмотреть возможность назначения глюкокортикостероида местного (ИГКС) в низкой дозе в ежедневном режиме или антагониста лейкотриеновых рецепторов (АЛР) с использованием бета-2-адреномиметика селективного (КДБА) по необходимости для купирования приступов астмы всем пациентам с легкой БА и наличием факторов риска обострения в качестве альтернативного подхода к лечению.
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии:
Подробнее о выборе доз ИГКС с учетом возраста см. Приложение А3.2, А3.3., А3.4. Лечение низкими дозами ИГКС является предпочтительным, особенно для детей младше 5 лет и должно продолжаться не менее 3-х месяцев. Для детей данной возрастной категории при выборе средства доставки следует руководствоваться доступностью, предпочтением родителей и возможностями пациента (спейсер либо небулайзер с маской или мундштуком).
Подробнее о выборе доз ИГКС с учетом возраста см. Приложение А3.2, А3.3., А3.4. Лечение низкими дозами ИГКС является предпочтительным, особенно для детей младше 5 лет и должно продолжаться не менее 3-х месяцев. Для детей данной возрастной категории при выборе средства доставки следует руководствоваться доступностью, предпочтением родителей и возможностями пациента (спейсер либо небулайзер с маской или мундштуком).
Альтернативным вариантом терапии является ежедневный прием анагонистов лейкотриеновых рецепторов.
За счет специфического связывания с цистеиниллейкотриеновыми рецепторами АЛР (монтелукаст) подавляют воспаление слизистой носа и бронхов, спровоцированное аллергеном и неспецифическими триггерами, обладают выраженным противоаллергическим и противовоспалительным действием, эффективны как в подавлении симптомов, так и с целью профилактики симптомов БА и аллергического ринита; АЛР уступают по эффективности ИГКС.
Могут применяться как в качестве монотерапии, так и в комплексной терапии БА. Однако, при отсутствии эффекта, прежде чем перейти на третью ступень лечения, рекомендуется рассмотреть назначение низких доз ИГКС [160].
За счет специфического связывания с цистеиниллейкотриеновыми рецепторами АЛР (монтелукаст) подавляют воспаление слизистой носа и бронхов, спровоцированное аллергеном и неспецифическими триггерами, обладают выраженным противоаллергическим и противовоспалительным действием, эффективны как в подавлении симптомов, так и с целью профилактики симптомов БА и аллергического ринита; АЛР уступают по эффективности ИГКС.
Могут применяться как в качестве монотерапии, так и в комплексной терапии БА. Однако, при отсутствии эффекта, прежде чем перейти на третью ступень лечения, рекомендуется рассмотреть назначение низких доз ИГКС [160].
Монтелукаст (код АТХ: R03DC03) детям в возрасте от 2 до 6 лет по 4 мг (1 жевательная таблетка) 1р в сутки; детям в возрасте от 6 до 15 лет по 5 мг (1 жевательная таблетка) 1р в сутки; взрослым и детям старше 15 лет по 10 мг 1 р в сутки.
• Рекомендуется рассмотреть назначение комбинированного бронходилатирующего средства (бета2-адреномиметика селективного и глюкокортикостероида местного, код АТХ R03AK) на регулярной основе пациентам старше 6 лет со средне-тяжелой БА с использованием бета-2-адреномиметика селективного (КДБА) по потребности для купирования приступов астмы (если им уже не назначен формотерол+ИГКС в режиме единого ингалятора) или рассмотреть возможность удвоения доз ИГКС на регулярной основе (в качестве альтернативного варианта) с использованием бета-2-адреномиметика селективного (КДБА) по потребности для
купирования приступов астмы [41,120,161-166].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Комментарии:
На третьей ступени терапии БА у взрослых и детей с 6 лет возможно рассмотреть увеличение дозы ИГКС до средней (альтернативный вариант терапии), однако, это менее эффективно, чем добавление ДДБА. Комбинация низких доз ИГКС с АЛР или добавление низких доз теофиллина (альтернативный вариант терапии) с длительным высвобождением являются менее эффективными.
Комментарии:
На третьей ступени терапии БА у взрослых и детей с 6 лет возможно рассмотреть увеличение дозы ИГКС до средней (альтернативный вариант терапии), однако, это менее эффективно, чем добавление ДДБА. Комбинация низких доз ИГКС с АЛР или добавление низких доз теофиллина (альтернативный вариант терапии) с длительным высвобождением являются менее эффективными.
Подробнее о выборе средних доз ИГКС с учетом возраста см. Приложение А3.2, А3.3, А3.4.
Важно предупредить пациента о том, что количество ингаляций КДБА по необходимости не должно превышать 6 инг/сут.
Кроме ранее упомянутых комбинаций ИГКС+ДДБА, которые могут быть рекомендованы в режиме единого ингалятора (Будесонид + формотерол** код АТХ: RO3AKO7; Беклометазон + формотерол**, код АТХ: RO3AKO8 и Беклометазон + сальбутамол, код АТХ: RO3AKO8), в данной группе можно рассмотреть назначение:
Будесонид + формотерол** (код АТХ: RO3AKO7) в дозированном аэрозольном ингаляторе детям от 6 лет и взрослым 80/4,5 мкг по 2 инг * 1-2 в день, подросткам с 12 лет и взрослым возможно 160/4,5 мкг по 2 инг * 1-2 р в день на регулярной основе
Салметерол + флутиказон** (код АТХ: R03AK06) в дозированном аэрозольном ингаляторе детям от 4 до 12 лет 25/50 мкг * 2 р в день, взрослым и подросткам от 12 лет 50/100 мкг или 50/250 мкг * 2 р в день на регулярной основе или в дозированном порошковом ингаляторе взрослым и подросткам от 12 лет 50/100 мкг или 50/250 мкг * 2 р в день на регулярной основе
Вилантерол + флутиказона фуроат** (код АТХ: R03AK10) в дозированном порошковом ингаляторе взрослым и подросткам от 12 лет 22/92 мкг * 1 р в день на регулярной основе.
Также, возможные к назначению комбинации ИГКС+ДДБА как мометазон+формотерол (код АТХ: R03AK09) и мометазон+индакатерол (код АТХ: R03AK14), в настоящее время временно недоступны на территории РФ.
• Рекомендуется рассмотреть возможность удвоения доз ИГКС на регулярной основе пациентам младше 5 лет со средне-тяжелой БА с использованием селективного бета-2-адреномиметика (КДБА) по потребности..
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии:
Подробнее о выборе средних доз ИГКС с учетом возраста см. Приложение А3.2, А3.3, А3.4.
Прежде чем приступать к более активному лечению – перейти на 3 ступень терапии, необходимо убедиться, что симптомы вызваны БА, а не сопутствующим или альтернативным заболеванием. В качестве альтернативного варианта терапии возможно рассмотреть добавление к низким дозам ИГКС АЛР.
Комментарии:
Подробнее о выборе средних доз ИГКС с учетом возраста см. Приложение А3.2, А3.3, А3.4.
Прежде чем приступать к более активному лечению – перейти на 3 ступень терапии, необходимо убедиться, что симптомы вызваны БА, а не сопутствующим или альтернативным заболеванием. В качестве альтернативного варианта терапии возможно рассмотреть добавление к низким дозам ИГКС АЛР.
Использование ИГКС+ДДБА у детей младше 4 лет на третьей ступени терапии не рекомендовано, так как их безопасность и эффективность мало изучены в данной возрастной группе, а данное назначение будет вне инструкции.
В одном исследовании не было выявлено статистически значимых различий в эффективности ИГКС+ДДБА и монотерапии ИГКС у пациентов младше 4 лет.
В одном исследовании не было выявлено статистически значимых различий в эффективности ИГКС+ДДБА и монотерапии ИГКС у пациентов младше 4 лет.
• Рекомендуется рассмотреть возможность назначения фиксированной тройной комбинации ИГКС+ДДБА+ДДАХ (бета2-адреномиметика селективного и глюкокортикостероида местного, код АТХ R03AL) пациентам старше 18 лет с неконтролируемой БА несмотря на терапию средними и высокими дозами ИГКС в комбинации с ДДБА и наличием одного и более обострений за последний год (в качестве предпочтительной терапии).
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии:
У взрослых пациентов с недостаточным контролем над БА на фоне средних доз ИГКС+ДДБА, назначение фиксированной тройной комбинации ИГКС+ДДБА+ДДАХ улучшает функцию легких и снижает частоту обострений.
Комментарии:
У взрослых пациентов с недостаточным контролем над БА на фоне средних доз ИГКС+ДДБА, назначение фиксированной тройной комбинации ИГКС+ДДБА+ДДАХ улучшает функцию легких и снижает частоту обострений.
Вилантерол + умеклидиния бромид + флутиказона фуроат** (код АТХ: R03AL08) в дозированном порошковом ингаляторе взрослым 22/55/92 мкг или 22/55/184 мкг по 1 инг * 1 р в день на регулярной основе.
Беклометазон + гликопиррония бромид + формотерол (код АТХ: R03AL09) в дозированном аэрозольном ингаляторе взрослым 100/10/6 мкг по 2 инг * 2 р в день на регулярной основе.
Гликопиррония бромид + индакатерол + мометазон (код АТХ: R03AL12) в капсулах с порошком и устройством для ингаляций взрослым 50/150/80 мкг или 50/150/160 мкг по 1 инг * 1 р в день на регулярной основе.
• Рекомендуется рассмотреть возможность добавления антихолинергического средства (ДДАХ) тиотропия бромида** к средним или высоким дозам ИГКС в комбинации с ДДБА (бета2-адреномиметика селективного и глюкокортикостероида местного, код АТХ R03AL) пациентам старше 6 лет с неконтролируемой БА, несмотря на терапию средними и высокими дозами ИГКС в комбинации с ДДБА (в качестве предпочтительной терапии).
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии:
Несмотря на то, что тиотропия бромид** доступен в виде разных ингаляционных устройств, данные по использованию препарата при БА получены только для жидкостного ингалятора и не могут быть экстраполированы на тиотропия бромид** в виде ДПИ. Для лечения БА из длительнодействующих антихолинергических препаратов зарегистрирован только тиотропия бромид**.
Комментарии:
Несмотря на то, что тиотропия бромид** доступен в виде разных ингаляционных устройств, данные по использованию препарата при БА получены только для жидкостного ингалятора и не могут быть экстраполированы на тиотропия бромид** в виде ДПИ. Для лечения БА из длительнодействующих антихолинергических препаратов зарегистрирован только тиотропия бромид**.
Тиотропия бромид** (код АТХ: R03BB04) р-р для ингаляции в комплекте с ингалятором детям от 6 лет и взрослым 2,5 мкг по 2 инг * 1р в день.
• Рекомендуется рассмотреть возможность назначения высоких доз ИГКС в комбинации с ДДБА (бета2-адреномиметика селективного и глюкокортикостероида местного, код АТХ R03AK) на регулярной основе пациентам старше 12 лет при недостаточной эффективности средних доз ИГКС в комбинации с ДДБА или добавление АЛР в качестве альтернативной терапии.
Уровень убедительности рекомендаций — B (уровень достоверности доказательств — 3)
Комментарии: эффективность подобной тактики уступает добавлению к терапии ДДАХ.
Также возможно повышение кратности приема средней/высокой дозы будесонида** до 4 раз в сутки, однако может отмечаться низкая приверженность к лечению.
Комментарии: эффективность подобной тактики уступает добавлению к терапии ДДАХ.
Также возможно повышение кратности приема средней/высокой дозы будесонида** до 4 раз в сутки, однако может отмечаться низкая приверженность к лечению.
• Рекомендуется у детей младше 5 лет при отсутствии контроля над БА на фоне удвоенной дозы ИГКС провести контроль техники ингаляции, приверженности к лечению, оценить вероятность воздействия факторов окружающей среды, исключить альтернативный диагноз.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии:
Оптимальное лечение для детей данного возраста в настоящий момент отсутствует.
Если диагноз БА подтвержден, то возможно применение следующих подходов: дальнейшее увеличение дозы ИГКС в течение нескольких недель до установления контроля над БА с отслеживанием побочных эффектов; добавление АЛР; назначение ИГКС+ДДБА (детям в возрасте ≥4 лет); периодическое добавление высоких доз ИГКС к ежедневной дозе базисной терапии в начале ОРИ; добавление низкой дозы СГКС в течение нескольких недель до установления контроля над симптомами БА с отслеживанием побочных эффектов.
Комментарии:
Оптимальное лечение для детей данного возраста в настоящий момент отсутствует.
Если диагноз БА подтвержден, то возможно применение следующих подходов: дальнейшее увеличение дозы ИГКС в течение нескольких недель до установления контроля над БА с отслеживанием побочных эффектов; добавление АЛР; назначение ИГКС+ДДБА (детям в возрасте ≥4 лет); периодическое добавление высоких доз ИГКС к ежедневной дозе базисной терапии в начале ОРИ; добавление низкой дозы СГКС в течение нескольких недель до установления контроля над симптомами БА с отслеживанием побочных эффектов.
3.1.1.1 Генно-инженерные биологические препараты (ГИБП) из фармакологической группы R03DX
«Прочие средства системного действия для лечения обструктивных заболеваний дыхательных путей»
• Рекомендуется пациентам в возрасте от 6 лет и старше с тяжелой БА рассмотреть возможность назначения генно-инженерных биологических препаратов (ГИБП) из фармакологической группы R03DX «Прочие средства системного действия для лечения обструктивных заболеваний дыхательных путей» или D11AH «Препараты для лечения дерматита, кроме
кортикостероидов» с учетом фенотипа БА в качестве дополнения к базисной терапии с целью достижения контроля над симптомами заболевания, снижения риска обострений и потребности в системных глюкокортикостероидах.
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Комментарии:
Эффекты применяемых на сегодняшний день ГИБП в терапии тяжелой БА сводятся к достижению контроля над симптомами, снижению частоты обострений, госпитализаций, посещения отделений неотложной помощи и потребности в ОКС (вплоть до полной отмены ОКС у пациентов, принимавших их на постоянной основе). Ответ на терапию ГИБП зависит от фенотипа БА, поэтому выбор правильного биологического препарата имеет решающее значение для обеспечения успеха терапии. Критериями отбора для биологической терапии в случае Т2-астмы служат биологические (наличие атопии, эозинофилия крови и мокроты; уровень сывороточного IgE; высокие уровни FeNO) и клинические маркеры (частота обострений, хороший ответ на терапию СГКС, наличие сопутствующих заболеваний, таких как рецидивирующий полипозный риносинусит, атопический дерматит) [194–207].
Комментарии:
Эффекты применяемых на сегодняшний день ГИБП в терапии тяжелой БА сводятся к достижению контроля над симптомами, снижению частоты обострений, госпитализаций, посещения отделений неотложной помощи и потребности в ОКС (вплоть до полной отмены ОКС у пациентов, принимавших их на постоянной основе). Ответ на терапию ГИБП зависит от фенотипа БА, поэтому выбор правильного биологического препарата имеет решающее значение для обеспечения успеха терапии. Критериями отбора для биологической терапии в случае Т2-астмы служат биологические (наличие атопии, эозинофилия крови и мокроты; уровень сывороточного IgE; высокие уровни FeNO) и клинические маркеры (частота обострений, хороший ответ на терапию СГКС, наличие сопутствующих заболеваний, таких как рецидивирующий полипозный риносинусит, атопический дерматит) [194–207].
Решение вопроса о назначении и выборе ГИБП принимает врачебный консилиум специалистов, имеющих опыт в проведении терапии ГИБП при БА.
В настоящее время для лечения тяжелой неконтролируемой БА существует несколько ГИБП:
Омализумаб** (код АТХ: R03DX05) разрешен к применению у детей от 6 лет и взрослых, расчет дозы (от 75 мг до 600 мг) и схемы применения (подкожно каждые 2 или 4 нед) производится в зависимости от исходного уровня общего иммуноглобулина Е и массы тела пациента, согласно таблице в инструкции.
Дупилумаб** (код АТХ: D11AH05) разрешен к применению у детей от 6 лет и взрослых; для детей от 12 лет и взрослых начальная доза — 400 мг подкожно (2 инъекции по 200 мг), далее — по 200 мг каждые 2 недели; для пациентов с глюкокортикостероидозависимой БА или сопутствующим среднетяжелым или тяжелым атопическим дерматитом, при котором показано применение препарата начальная доза — 600 мг (2 инъекции по 300 мг), далее — по 300 мг каждые 2 недели. Для детей от 6 до 11 лет: с массой тела от 15 <30 кг начальная и последующие дозы 300 мг каждые 4 нед, с массой тела от 30 <60 кг начальная и последующие дозы 200 мг каждые 2 нед, или 300 мг каждые 4 нед; с массой тела ≥60 кг начальная и последующие дозы 200 мг каждые 2 нед. Для детей от 6 до 11 лет с сопутствующим среднетяжелым или тяжелым атопическим дерматитом: с массой тела от 15 <30 кг начальная доза 600 мг, далее по 300 мг каждые 4 нед, с массой тела от 30 <60 кг начальная доза 400 мг, далее по 200 мг каждые 2 нед; с массой тела ≥60 кг начальная доза 600 мг, далее по 300 мг каждые 2 нед.
Меполизумаб** (код АТХ: R03DX09) разрешен к применению у детей от 6 лет и взрослых, детям от 6 до 12 лет 40 мг подкожно 1 раз каждые 4 недели, 12 лет и старше 100 мг 1 раз каждые 4 недели.
Реслизумаб** (код АТХ: R03DX08) разрешен к применению у взрослых (с 18 лет) из расчета 3 мг/кг веса внутривенно 1раз каждые 4 недели.
Бенрализумаб** (код АТХ: R03DX10) разрешен к применению у взрослых (с 18 лет) 30 мг подкожно каждые 4 недели 3 раза, затем каждые 8 недель.
Тезепелумаб (код АТХ: R03DX11) разрешен к применению у детей с 12 лет и взрослых 210 мг подкожно 1раз каждые 4 недели.
Комментарии:
Омализумаб** (гуманизированное моноклональное антитело против IgE, разработанное на основе человеческого IgG1), связываясь с IgE антителами, блокирует их взаимодействие с высокоаффинными FcsRl-рецепторами, приводит к снижению концентрации IgE — пускового фактора каскада аллергических реакций. При применении омализумаба** у пациентов с атопической БА отмечается уменьшение количества FcsRl- рецепторов на поверхности базофилов, тучных клеток и дендритных клеток. Хороший ответ на добавление омализумаба** в базисную терапию можно ожидать у пациентов с клинически подтвержденной атопией и хорошим ответом на СГКС, ограничением может быть либо низкий (менее 30 МЕ/мл), либо
крайне высокий уровень общего иммуноглобулина E (более 1500 МЕ/мл) и большой вес тела, т.к. расчет дозы и режима терапии зависит от данных параметров.
Назначение ГИБП, являющихся блокаторами ИЛ-5 (меполизумаб**, реслизумаб**) или рецепторов к нему (анти-ИЛ-5Рα – бенрализумаб**), приводит к снижению уровня эозинофилов в периферической крови, слизистой дыхательных путей [43,195,196,198,202,209].
Хороший ответ на добавление препаратов этой группы можно ожидать у пациентов с эозинофильной ТБА с характерными маркерами эозинофильного воспаления, хорошим ответом на СГКС. Несмотря на схожий механизм действия препаратов этой группы ГИБП, имеются отличия в ограничениях по возрасту, исходному уровню эозинофилов периферической крови, способу введения и доказательной базе клинических исследований относительно возможности отмены ОКС.
Меполизумаб** — гуманизированное моноклональное антитело (IgG1κ), направленное против ИЛ-5, предотвращая его взаимодействие с a-цепью рецептора к ИЛ-5, экспрессируемого на клеточной поверхности эозинофилов, снижает количество эозинофилов и их предшественников в костном мозге и в слизистой оболочке дыхательных путей. Меполизумаб** нормализует уровень эозинофилов до физиологического у пациентов с тяжелой БА как аллергического, так и неаллергического генеза [77,195,196,201,203,209–211]. Показанием к применению меполизумаба** является тяжелая эозинофильная БА у пациентов старше 6 лет, уровень эозинофилов в периферической крови на момент начала терапии ≥150 клеток/мкл или ≥300 клеток/мкл в течение предшествующих 12 месяцев.
Реслизумаб** — гуманизированное моноклональное антитело (IgG4k) к человеческому ИЛ-5, нейтрализующее свободно циркулирующий цитокин и предотвращающее его связывание с эозинофилами. Показанием к применению реслизумаба** является тяжелая эозинофильная БА у пациентов старше 18 лет, уровень эозинофилов в периферической крови на момент начала терапии ≥400 клеток/мкл. Также особенностью препарат является внутривенный способ введения и необходимость расчета дозы в зависимости от массы тела пациента.
Бенрализумаб – афукозилированное гуманизированное моноклональное антитело (IgG1k), которое связывается с a-субъединицей рецептора к человеческому ИЛ-5 (ИЛ-5Рa), расположенного на поверхности эозинофилов и базофилов, с высоким сродством и специфичностью. Отсутствие остатков фукозы в Fc-домене бенрализумаба облегчает
процесс связывания с FcγRIIIa, низкой или средней аффинности рецепторами IIIa к Fcγ, на поверхности иммунных клеток, таких как натуральные киллеры, макрофаги и нейтрофилы. За счет высокой аффинности к FcγRIIIa и, как следствие, привлечения эффекторных клеток иммунитета к месту образования комплекса с ИЛ-5Рa, бенрализумаб запускает апоптоз эозинофилов и базофилов посредством антителозависимой клеточноопосредованной цитотоксичности [215,216]. Таким образом, бенрализумаб** может приводить к полному истощению пула эозинофилов эпителия дыхательных путей без их дегрануляции. Бенрализумаб** рекомендован взрослым пациентам (старше 18 лет) с тяжелой БА с эозинофильным фенотипом, уровнем эозинофилов в периферической крови ≥300 клеток/мкл, а также пациентам с гормонозависимой БА [202,204,215,216].
Дупилумаб** — человеческое моноклональное антитело (IgG4) к альфа-субъединице рецептора к ИЛ-4 (ИЛ-4Рα), идентичной альфа-субъединице рецептора к ИЛ-13 (ИЛ-13Рα). Селективное связывание дупилумабом** ИЛ-4Рa/ИЛ-13Рa предотвращает дальнейшее проведение сигналов с этих молекул, которые опосредуют процессы Т2-воспаления [24]. Дупилумаб** показан пациентам с ТБА, в основе патогенеза которой лежит Т2-воспаление, в том числе с гормонозависимой БА. Помимо показания для лечения ТБА дупилумаб** одобрен для терапии пациентов с тяжелым атопическим дерматитом (у детей с 6 мес), хроническим полипозным риносинуситом, эозинофильным эзофагитом, что позволяет также достигать контроля (при наличии) сопутствующих заболеваний с Т2-воспалением у пациентов с ТБА [197,199,202,217,218]. Ограничением может быть высокий исходный уровень эозинофилии периферической крови (более 1500 кл/мкл).
Тезепелумаб — человеческое моноклональное антитело (IgG2λ) к тимусному стромальному лимфопоэтину (ТСЛП) — цитокину эпителиального происхождения, играющего ключевую роль в инициировании и сохранении воспаления дыхательных путей, индуцировании бронхиальной гиперреактивности, оказывающего косвенное влияние на структурные клетки дыхательных путей (например, фибробласты и клетки гладкой мускулатуры дыхательных путей). Блокирование ТСЛП тезепелумабом снижает уровень широкого спектра биомаркеров и цитокинов, связанных с развитием воспаления (в том числе эозинофилов в крови, IgE, FeNO, ИЛ-5 и ИЛ-13) [200,204,205,219]. Доза препарата не зависит от исходного уровня эозинофилов в крови, других биомаркеров воспаления, а также наличия или отсутствия атопии.
Первичную оценку эффективности ГИБП осуществляют спустя 16 недель от начала терапии, при наличии эффекта (улучшение контроля БА) продолжать терапию выбранным ГИБП не менее 12 мес с последующей оценкой исходов. На сегодняшний день не существует доказательной базы по продолжительности терапии ГИБП.
Длительность курса определяет специалист на основании достигнутого уровня контроля над БА и сопутствующими аллергическими заболеваниями, с учетом снижения объема базисной терапии ИГКС. В ограниченных исследованиях было показано, что пациенты, продолжавшие биологическую терапию, имели лучшие клинические результаты, чем те, кто перешел на другую терапию или прекратил ее, что свидетельствует о важности правильного выбора исходного биологического препарата и продолжения терапии.
Длительность курса определяет специалист на основании достигнутого уровня контроля над БА и сопутствующими аллергическими заболеваниями, с учетом снижения объема базисной терапии ИГКС. В ограниченных исследованиях было показано, что пациенты, продолжавшие биологическую терапию, имели лучшие клинические результаты, чем те, кто перешел на другую терапию или прекратил ее, что свидетельствует о важности правильного выбора исходного биологического препарата и продолжения терапии.
• Рекомендуется пациентам с тяжелой БА, неконтролируемой объемом терапии, соответствующим 5 ступени, рассмотреть вопрос о назначении кортикостероидов системного действия (СГКС, код АТХ Н02А) в качестве дополнения к базисной терапии с целью достижения контроля над симптомами заболевания, снижения риска обострений и улучшения функции легких [20].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии:
Назначение СГКС следует рассматривать как терапию «отчаяния» — исключительную стратегию в случае отсутствия контроля над симптомами и/или частых обострений, несмотря на правильную технику ингаляции и хорошую приверженность на 5 ступени лечения.
Должны быть исключены факторы, способствующие персистированию симптомов и возникновению обострений, если другие методы терапии, включая биологическую, не показали свою эффективность у конкретного пациента.
Рекомендуемая доза системных кортикостероидов — ≤7,5 мг/сут в преднизолоновом эквиваленте. лечение для детей данного возраста в настоящий момент отсутствует.
Комментарии:
Назначение СГКС следует рассматривать как терапию «отчаяния» — исключительную стратегию в случае отсутствия контроля над симптомами и/или частых обострений, несмотря на правильную технику ингаляции и хорошую приверженность на 5 ступени лечения.
Должны быть исключены факторы, способствующие персистированию симптомов и возникновению обострений, если другие методы терапии, включая биологическую, не показали свою эффективность у конкретного пациента.
Рекомендуемая доза системных кортикостероидов — ≤7,5 мг/сут в преднизолоновом эквиваленте. лечение для детей данного возраста в настоящий момент отсутствует.
Преднизолон** (код АТХ: H02AB06) доза и продолжительность лечения устанавливается врачом индивидуально в зависимости от показаний и тяжести заболевания
Метилпреднизолон** (код АТХ: H02AB04) доза и продолжительность лечения устанавливается врачом индивидуально в зависимости от показаний и тяжести заболевания
Дексаметазон** (код АТХ: H02AB02) доза и продолжительность лечения устанавливается врачом индивидуально в зависимости от показаний и тяжести заболевания
• Рекомендуется взрослым пациентам с сохраняющимися симптомами БА, на фоне терапии высокими дозами ИГКС+ДДБА и биологическими препаратами (или СГКС) рассмотреть вопрос о назначении #азитромицина** в качестве противовоспалительной терапии с целью достижения контроля над симптомами [20,222-226].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии:
Макролиды являются антибактериальными препаратами с доказанной противовоспалительной активностью.
Проведенный Hiles SA с соавт. [224] систематический обзор и метаанализ подтверждают, что добавление #азитромицина** к базисной терапии плохо контролируемой БА снижает количество обострений как при эозинофильном, так и при неэозинофильном фенотипе БА, а также потребность в СГКС.
Однако, данные о влиянии #азитромицина** на качество жизни пациентов с БА противоречивы, а воздействия на функцию легких (ОФВ1) практически не отмечено.
Комментарии:
Макролиды являются антибактериальными препаратами с доказанной противовоспалительной активностью.
Проведенный Hiles SA с соавт. [224] систематический обзор и метаанализ подтверждают, что добавление #азитромицина** к базисной терапии плохо контролируемой БА снижает количество обострений как при эозинофильном, так и при неэозинофильном фенотипе БА, а также потребность в СГКС.
Однако, данные о влиянии #азитромицина** на качество жизни пациентов с БА противоречивы, а воздействия на функцию легких (ОФВ1) практически не отмечено.
#Азитромицин** (код АТХ: J01FA10) назначают трижды в неделю по 500 мг на срок не менее, чем 6 мес.
Перед назначением препарата необходимо проведение микробиологического исследования мокроты на наличие атипичных микобактерий (Микробиологическое (культуральное)
Перед назначением препарата необходимо проведение микробиологического исследования мокроты на наличие атипичных микобактерий (Микробиологическое (культуральное)
исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы и/или Микробиологическое (культуральное) исследование мокроты на аэробные и факультативно-анаэробные микроорганизмы с использованием автоматизированного оборудования, Определение чувствительности микроорганизмов к антимикробным
химиотерапевтическим препаратам), электрокардиографии для исключения удлиненного интервала QT.
