У пациентов с СД некоторые заболевания и состояния (например, сердечно-сосудистые заболевания) имеют отличия от лиц без СД, что должно быть учтено при определении тактики ведения. Лечение пациентов с СД пожилого возраста и во время беременности имеет особенности как при выборе индивидуальных целей лечения, так и оптимальных (безопасных) схем терапии.
7.1 . Острые осложнения (неотложные состояния) Подробная диагностика, клиника и лечение острых осложнений СД 2 изложены в соответствующих клинических рекомендациях.
Клиника, диагностика и лечение гипогликемии изложены в разделе 3.6 Гипогликемия.
7.2 Диабетическая нефропатия Диабетическая нефропатия (ДН) – специфическое поражение почек при сахарном диабете в виде узелкового гломерулосклероза как результат воздействия метаболических и гемодинамических факторов на почечную микроциркуляцию, модулируемый генетическими факторами.
Хроническая болезнь почек (ХБП) – наднозологическое понятие, определяется как нарушение структуры или функции почек, сохраняющееся более 3 месяцев и имеющее последствия для здоровья.
ДН развивается у 20-40% пациентов с СД 2, возможна диагностика осложнения одновременно с заболеванием.
Развитие ДН существенно повышает риск кардиоваскулярной патологии и стоимость лечения.
Согласно концепции ХБП, оценка стадии почечной патологии осуществляется по величине рСКФ, признанной как наиболее полно отражающей количество и суммарный объем работы нефронов, в том числе связанной с выполнением неэкскреторных функций (табл. 20). Кроме того, выделяют три категории альбуминурии (табл. 21).
Таблица 20. Стадии хронической болезни почек по уровню скорости клубочковой фильтрации
1Для установления ХБП в этом случае необходимо наличие также и маркеров почечного повреждения. При их отсутствии ХБП не диагностируется.
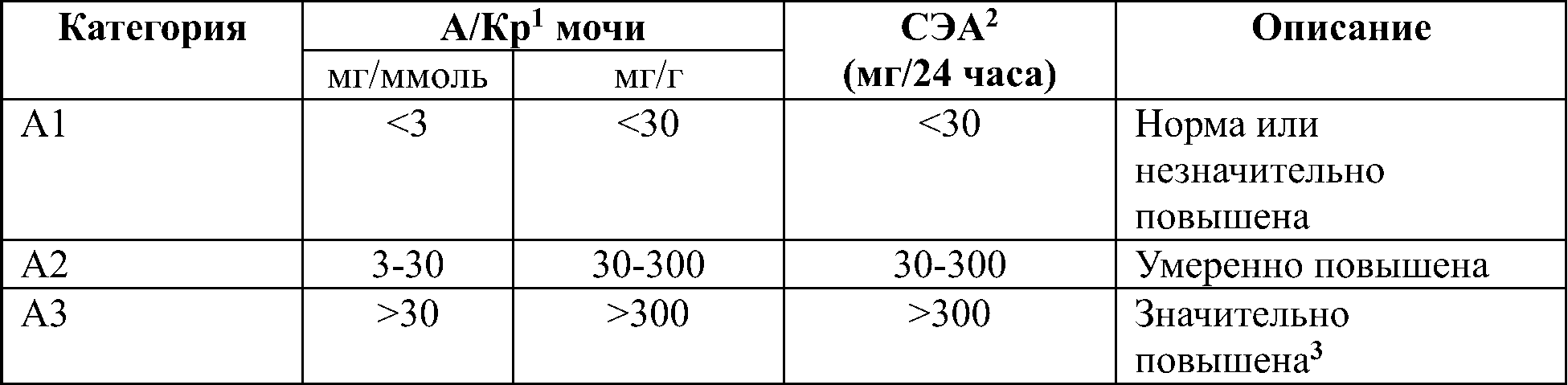
Таблица 21. Классификация хронической болезни почек по уровню альбуминурии
1 А/Кр – соотношение альбумин/креатинин в утренней порции мочи
2 СЭА – суточная экскреция альбумина
3 Включая нефротический синдром (СЭА >2200 мг/24 часа [А/Кр>2200 мг/г; >220 мг/ммоль])
Формулировка диагноза ДН в соответствии с классификацией ХБП:
> ДН, ХБП С1 (2, 3, 4 или 5) А2
> ДН, ХБП С1 (2, 3, 4 или 5) А3
> ДН, ХБП С3 (4 или 5) А1 (т.е. независимо от уровня альбуминурии);
> ДН, ХБП С5 (лечение заместительной почечной терапией);
> в случае нормализации показателей альбуминурии на фоне нефропротективной терапии у пациентов с сохранной рСКФ ≥ 60 мл/мин/1,73 м2 — диагноз ДН, ХБП сохраняется с формулировкой: ДН, ХБП С1-2 А1 (регресс альбуминурии на фоне нефропротективной терапии).
Специфические симптомы ДН на стадии ХБП С1-3 А1-2 отсутствуют у пациентов с СД 2.
На стадии ХБП С4-5 отмечают слабость, сонливость, быструю утомляемость, выраженные стойкие отеки, стабильно повышенное АД, тошноту, иногда рвоту без облегчения состояния.
На стадии ХБП С3-5 А3 отмечают отеки стоп, голеней, иногда бедер, лица, снижение аппетита, нарастание и постоянно повышенное АД.
Диагностика
• Рекомендуется оценка соотношения альбумин/креатинин (предпочтительно) или определение концентрации альбумина в разовой порции мочи и рСКФ всем пациентам с СД 2 при постановке диагноза СД, далее не реже 1 раза в год, для выявления ДН.
Комментарии:
Для пациентов с СД 2 и альбуминурией ≥ 3 мг/ммоль и/или рСКФ <60 мл/мин/1,73 м2 целесообразно проводить оценку этих показателей 2 раза в год.
Соотношение альбумин/креатинин в разовой (предпочтительно утренней) порции мочи с высокой чувствительностью и специфичностью соотносится с суточной экскрецией альбумина с мочой. Определение в разовой порции мочи только альбумина без креатинина не дает такого точного соотношения, так как не учитывает влияние разведения мочи в силу различной гидратации. Поскольку в клинической практике продолжается оценка в разовой порции мочи только альбумина, то результаты этого исследования необходимо интерпретировать следующим образом (значения, соответствующие уровням альбуминурии согласно классификации ХБП): не более 20 мг/л — А1; >20 до 200 мг/л — А2; > 200 мг/л — А3.
• Рекомендуется оценка потенциальных осложнений ХБП пациентам с СД 2 и рСКФ < 60 мл/мин/1,73 м2 (АГ, электролитные нарушения, метаболический ацидоз, анемия, минеральные и костные нарушения) для своевременной инициации терапии.
• Рекомендуется незамедлительное обращение пациентов с СД 2 к врачу-нефрологу при быстром прогрессировании почечной патологии для определения этиологии и терапии.
Комментарии: Диагностика ДН основывается на наличии повышенной альбуминурии и/или снижении рСКФ при отсутствии симптомов первичной почечной патологии.
Повреждение почек у пациентов с СД 2, как правило, имеет сложный (многофакторный) генез.
У пациентов с СД 2 ДН может диагностироваться и при отсутствии ДР (умеренно чувствительный и специфический маркер), а также при снижении рСКФ на фоне нормоальбуминурии.
С учетом вариабельности для установления диагноза ДН необходимо не менее, чем 2-кратное исследование соотношения альбумин/креатинин или концентрации альбумина в разовой порции мочи (только количественными методами) и рСКФ в период от 1 до 3 мес.
Преходящее повышение экскреции альбумина с мочой возможно при значительной гипергликемии, интенсивной физической нагрузке, высокобелковом питании, лихорадке, менструации. рСКФ вычисляется с учетом уровня креатинина плазмы с использованием валидизированной формулы (предпочтительно формула CKD-EPI, наилучшим образом соотносящаяся с референтными (клиренсовыми) методами определения). Определение СКФ клиренсовыми методами необходимо при беременности, морбидном ожирении (ИМТ >40 кг/м2), дефиците массы тела (ИМТ <15 кг/м2), вегетарианстве, миодистрофии, параплегии, квадриплегии, нестандартных размерах тела (ампутированные конечности), остром почечном повреждении, почечном трансплантате, назначении нефротоксичных препаратов, определении начала заместительной почечной терапии. При быстро нарастающей альбуминурии, внезапном развитии нефротического синдрома, быстром снижении рСКФ, изменении осадка мочи (гематурия, лейкоцитурия, цилиндрурия) можно предположить альтернативную или дополнительную причину почечной патологии.
Лечение
• Рекомендуется потребление белка не более 0,8 г/кг массы тела в сутки недиализным небеременным пациентам с СД 2 и ХБП 3-5 для замедления прогрессирования ДН.
Комментарии:
Потребление такого количества белка в сравнении с большим уровнем замедляет снижение рСКФ. Диета, содержащая более 1,3 г/кг/сут ассоциирована с усилением альбуминурии, быстрым снижением почечной функции, кардиоваскулярной смертностью. Потребление белка не более 0,8 г/кг/сут не влияет на контроль гликемии, кардиоваскулярный риск и снижение рСКФ. Для пациентов на диализе необходимо более высокое потребление белка, так как нарушение питательного статуса — важная проблема диализных пациентов.
• Рекомендуется ограничение потребления натрия до 2,3 г/сут пациентам с СД 2 и ХБП для контроля АД, снижения кардиоваскулярного риска.
Комментарии: 2,3 г натрия соответствует 5 г поваренной соли.
• Рекомендуется ограничение потребления калия пациентам с СД 2 и ХБП для снижения риска гиперкалиемии.
Комментарии:
Потребление натрия и калия необходимо индивидуализировать с учетом коморбидности, применяемых препаратов, уровня АД и лабораторных данных
• Рекомендуется физическая активность умеренной интенсивности соответственно сердечно-сосудистой и физической толерантности пациентам с СД 2 и ХБП для снижения риска прогрессирования ДН.
Комментарии:
У лиц с СД 2 и ХБП, как и в общей популяции, регулярная и достаточная физическая активность обеспечивает кардиометаболические, ренальные и когнитивные преимущества, повышает качество жизни, улучшает чувствительность к инсулину, понижает уровень маркеров воспаления и улучшает функцию эндотелия. Однако, пациенты с ХБП имеют ограничения, препятствующие участию в регулярных упражнениях и в деятельности высокой интенсивности, прежде всего, связанные с возрастом и, следовательно, с риском падения. Потеря мышечной массы и развитие таких осложнений, как анемия, периферическая нейропатия, автономная нейропатия, лимитируют функциональные способности этих пациентов, параллельно снижению почечной функции. Несмотря на такие ограничения, рекомендация физической активности во время обычного визита важна для пациентов практически во всех ситуациях, несмотря на конкурирующие проблемы и недостаток конкретных ресурсов. До реализации программы физической активности необходимо провести оценку физической толерантности, риска нежелательных явлений (прежде всего, падения), а также доступности с учетом выраженности АССЗ.
• Рекомендуется оптимизировать контроль гликемии пациентам с СД 2 для снижения риска или замедления прогрессирования ХБП .
Комментарии:
У пациентов с выраженными стадиями ХБП целевой уровень HbAic должен быть индивидуализирован с учетом высокого риска гипогликемии.
Метформин** рассматривается как первый препарат для всех пациентов с СД 2, включая лиц с ХБП.
Метформин** противопоказан пациентам с СД 2 и ХБП при рСКФ < 30 мл/мин/1,73 м2.
На фоне терапии метформином** необходим мониторинг рСКФ; переоценка (титрация) дозы при рСКФ < 45 мл/мин/1,73 м2.
Не рекомендуется инициировать терапию метформином** при рСКФ < 45 мл/мин/1,73 м2.
Прием метформина** прекращается при проведении исследований с в/в введением йодсодержащих рентгеноконтрастных препаратов ввиду возможной концентрации препарата и последующего развития лактатацидоза.
Исследования ADVANCE и ADVANCE-ON показали, что достижение оптимального гликемического контроля с использованием препарата гликлазид** с модифицированным высвобождением приводит к снижение риска развития и прогрессирования ДН на 21%, снижение риска терминальной стадии ХБП на 65% у лиц СД 2 .
Выбор других сахароснижающих препаратов и их дозы у пациентов с СД 2 и ХБП определяется рСКФ, риском гипогликемии и прогрессирования ХБП, кардиоваскулярной патологией
(табл. 12 и 14 в разделе 3.4 Медикаментозная терапия).
• Рекомендуется применение иНГЛТ-2 у пациентов с СД 2 и ХБП с рСКФ>30 мл/мин/1,73 м2 для снижения риска прогрессирования ХБП и кардиоваскулярных событий .
Комментарии:
иНГЛТ-2 следует рассматривать для пациентов с СД 2 и ХБП как препараты дополнительно к метформину** для достижения целевого уровня контроля гликемии или как альтернативные в случае непереносимости или наличия противопоказаний к метформину**. Ряд крупных рандомизированных исследований этих препаратов у пациентов с СД 2 и установленными АССЗ или факторами риска АССЗ (EMPA-REG OUTCOME, CANVAS, DECLARE-TIMI 58, VERTIS CV) наряду с кардиоваскулярными исходами оценивали почечные исходы в качестве вторичных конечных точек. Эмпаглифлозин** значимо снижал риск развития или прогрессирования нефропатии на 39%, удвоения креатинина плазмы при соответствующей рСКФ ≤ 45 мл/мин/1,73 м2 на 44% в сравнении с плацебо.
Канаглифлозин значимо снижал риск прогрессирования альбуминурии на 27% и риск снижения рСКФ, достижения терминальной почечной недостаточности или ренальной смерти на 40% в сравнении с плацебо.
Дапаглфлозин** значимо снижал совокупность падения рСКФ ≥40% до < 60 мл/мин/1,73 м2, развития терминальной почечной недостаточности или почечной смерти на 47% в сравнении с плацебо.
Эртуглифлозин** показал в исследовательской вторичной ренальной точке, включавшей удвоение креатинина плазмы, инициацию заместительной почечной терапии, ренальную смерть, трендовое различие, однако более широкий анализ ренальных исходов, включавший оценку рСКФ (устойчивое снижение на 40%), т.е. сопоставимый с вышеприведенными исследованиями, показал значимое преимущество по конечной ренальной точке (снижение риска на 34% в сравнении с плацебо), как и в других исследованиях иНГЛТ-2.
Плацебо-контролируемое исследование CREDENCE показало значимое преимущество ренальных исходов в качестве первичной конечной точки у пациентов с СД 2 и ХБП на фоне терапии канаглифлозином. Плацебо-контролируемое исследование DAPA-CKD продемонстрировало значимое преимущество по снижению первичной конечной точки (стойкое снижение рСКФ ≥50%, терминальная почечная недостаточность, почечная или сердечнососудистая смерть) на фоне терапии дапаглифлозином** у пациентов с ХБП независимо от наличия СД 2 или его отсутствия при максимально переносимой блокаде ренин-ангиотензин-альдостероновой системы [326]. В дополнение к почечным эффектам иНГЛТ-2 демонстрируют кардиоваскулярные преимущества.
• Рекомендуется применение арГПП-1 (лираглутид, дулаглутид**, семаглутид**) у пациентов с СД 2 и ХБП с высоким риском кардиоваскулярных событий для снижения риска прогрессирования ХБП и кардиоваскулярных событий.
Комментарии:
арГПП-1 следует рассматривать для пациентов с СД 2 и ХБП с высоким риском кардиоваскулярных событий как препараты дополнительно к метформину** для достижения целевого уровня контроля гликемии или как альтернативные в случае непереносимости или наличия противопоказаний к метформину** и иНГЛТ-2. Ряд крупных рандомизированных исследований этих препаратов у пациентов с СД 2 и установленными АССЗ или факторами риска АССЗ (LEADER, SUSTAIN-6, REWIND) наряду с кардиоваскулярными исходами оценивали почечные исходы в качестве вторичных конечных точек. Лираглутид значимо снижал риск развития или прогрессирования нефропатии (совокупность возникновения стойкой макроальбуминурии, удвоения креатинина плазмы, развития терминальной почечной недостаточности, ренальной смерти) на 22% в сравнении с плацебо [161]. Семаглутид** значимо снижал риск развития или прогресс развития нефропатии (совокупность возникновения стойкой альбуминурии (соотношение альбумин/креатинин мочи > 30 мг/ммоль), удвоения креатинина плазмы, развития терминальной почечной недостаточности) на 36%.
Дулаглутид** значимо снижал совокупность развития стойкой макроальбуминурии (соотношение альбумин/креатинин мочи >33,9 мг/ммоль), стойкого снижения рСКФ на 30% и более и инициации заместительной почечной терапии на 15% [149]. В дополнение к почечным эффектам и арГПП-1 демонстрируют кардиоваскулярные преимущества. арГПП-1 (лираглутид, дулаглутид**, семаглутид**) могут использоваться прирСКФ > 15 мл/мин/1,73 м2 с большим преимуществом для снижения ССЗ, чем для прогрессирования ХБП и ХСН.
• Рекомендуется оптимизировать контроль АД пациентам с СД 2 для снижения риска или замедления прогрессирования ХБП.
• Рекомендуется прием ингибиторов ангитензинпревращающего фермента (иАПФ) или блокаторов рецепторов ангиотензина II (БРА) для небеременных пациентов с СД 2 и АГ, и/или повышенным соотношением альбумин/креатинин в моче ≥ 3 мг/ммоль и/или рСКФ < 60 мл/мин/1,73 м2 для замедления прогрессирования ХБП .
Комментарии: Режим дозирования иАПФ и БРА должен быть индивидуальным с учетом показателей рСКФ пациента и особенностей фармакокинетики препарата, указанных в инструкции.
• Рекомендуется контроль креатинина и калия сыворотки крови пациентам с СД 2, получающим иАПФ или БРА и диуретики (АТХ-классификация С03) для оценки безопасности терапии .
• Рекомендуется контроль соотношения альбумин/креатинин мочи пациентам с СД 2 с альбуминурией, получающим иАПФ или БРА для оценки эффективности лечения и прогрессирования .
• Не рекомендуется прием иАПФ или БРА пациентам с СД 2 при нормальном АД, соотношении альбумин/креатинин мочи < 3 мг/ммоль, нормальной рСКФ для первичной профилактики ХБП.
• Не рекомендуется комбинированная терапия иАПФ и БРА пациентам с СД 2 и ХБП во избежание гиперкалиемии или острого почечного повреждения.
Комментарии:
АГ — значимый фактор риска развития и прогрессирования ХБП. Антигипертензивная терапия снижает риск альбуминурии и кардиоваскулярных событий.
У пациентов с установленной ХБП (рСКФ < 60 мл/мин/1,73 м2 и/или соотношение альбумин/креатинин мочи > 30 мг/ммоль) иАПФ и БРА снижают риск прогрессирования до терминальной ХБП. Уровень АД менее 130/80 мм рт.ст. может рассматриваться как целевой на основе индивидуальных преимуществ и рисков. иАПФ и БРА — препараты первой линии для лечения АГ у пациентов с СД 2, АГ, рСКФ < 60 мл/мин/1,73 м2 и/или соотношением альбумин/креатинин мочи > 30 мг/ммоль, поскольку имеют доказанные преимущества по профилактике прогрессирования ХБП.
иАПФ и БРА имеют сопоставимые преимущества и риски.
При более низком уровне альбуминурии (соотношение альбумин/креатинин 3-30 мг/ммоль) терапия иАПФ и БРА демонстрирует снижение прогрессирования до более высокого уровня альбуминурии (соотношение альбумин/креатинин > 30 мг/ммоль) и кардиоваскулярных событий, но не прогрессирования до терминальной ХБП.
При отсутствии ХБП, иАПФ и БРА используются для контроля АД, но не имеют преимуществ по сравнению с другими классами антигипертензивных препаратов.
Антагонисты рецепторов минералокортикоидов (АТХ-классификация C03DA антагонисты альдостерона) (спиронолактон**, эплеренон) эффективны в лечении резистентной гипертензии, снижают альбуминурию по данным непродолжительных исследований пациентов с ХБП и могут иметь дополнительные кардиоваскулярные преимущества.
Однако они повышают эпизоды гиперкалиемии в двойной терапии (в комбинации с иАПФ или БРА).
Плацебо-контролируемое исследование FIDELIO-DKD показало значимое преимущество ренальных исходов в качестве первичной конечной точки (терминальная почечная недостаточность, снижение рСКФ >40%, ренальная смерть) у пациентов с СД 2 и ХБП на фоне терапии селективным антагонистом рецепторов минералокортикоидов.
• Рекомендуется терапия потенциальных осложнений ХБП у пациентов с СД 2 и рСКФ < 60 мл/мин/1,73 м2 для замедления их прогрессирования.
Комментарии: Подробные рекомендации по лечению осложнений ХБП (см. в соответствующих клинических рекомендациях).
• Рекомендуется определить сроки и возможности заместительной почечной терапии у пациентов с СД 2 и рСКФ < 30 мл/мин/1,73 м2 для ее плановой инициации.
Комментарии: Консультации врача-нефролога пациентов с СД 2 и ХБП С4 (рСКФ < 30 мл/мин/1,73 м2) могут снизить затраты, улучшить обслуживание и
отсрочить диализную терапию.
Профилактика ДН возможна только при своевременном определении и коррекции факторов риска развития и прогрессирования осложнения.
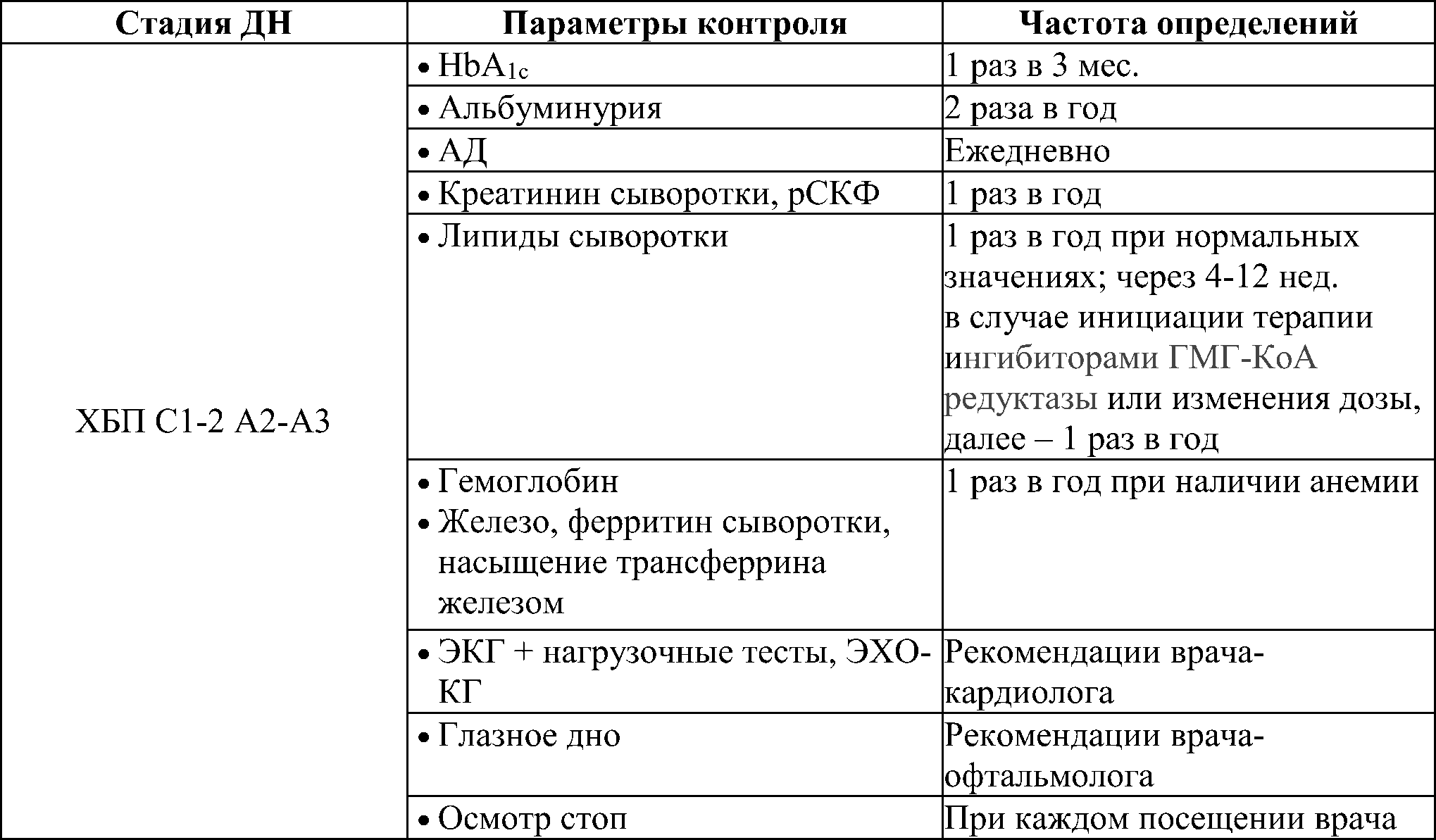
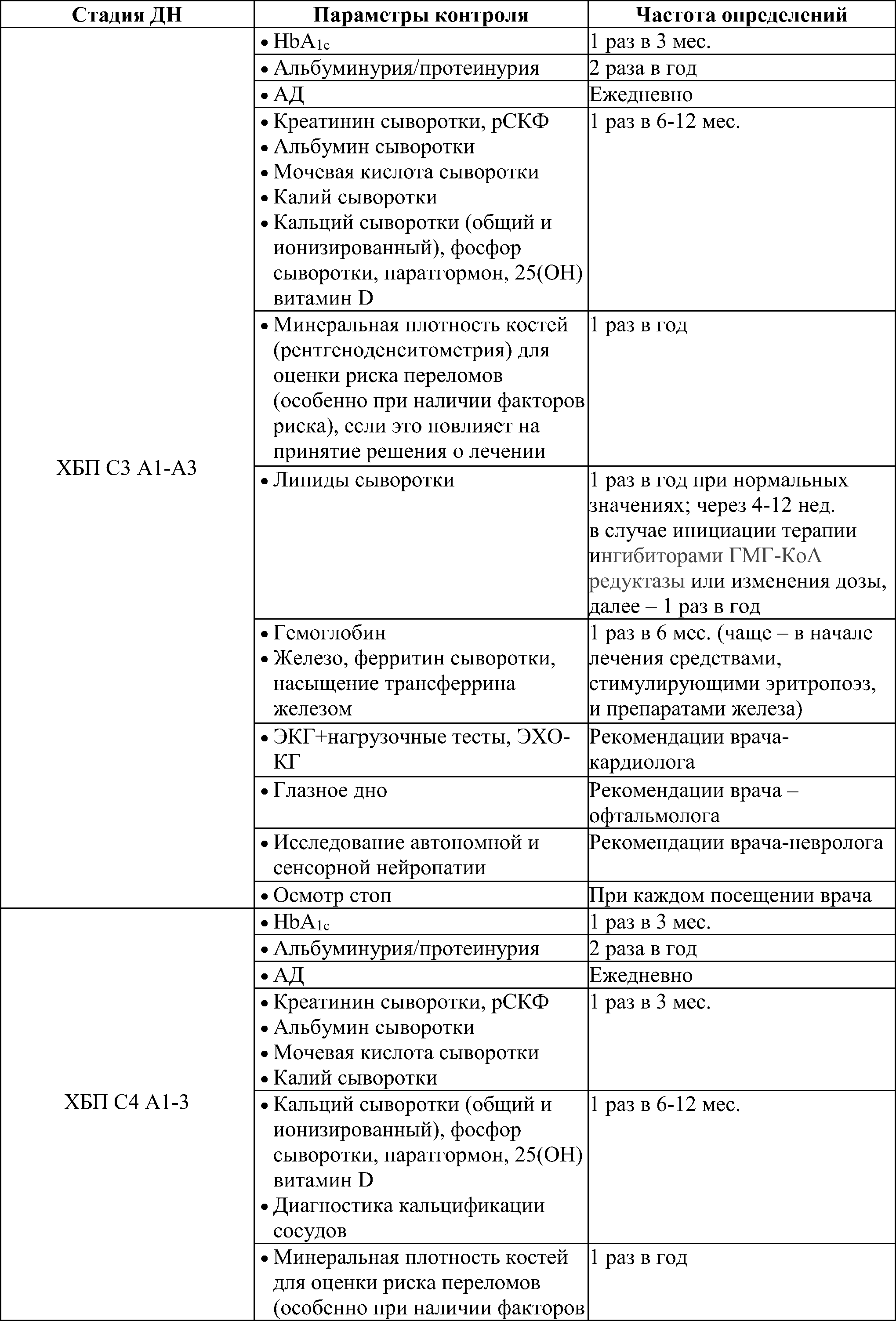
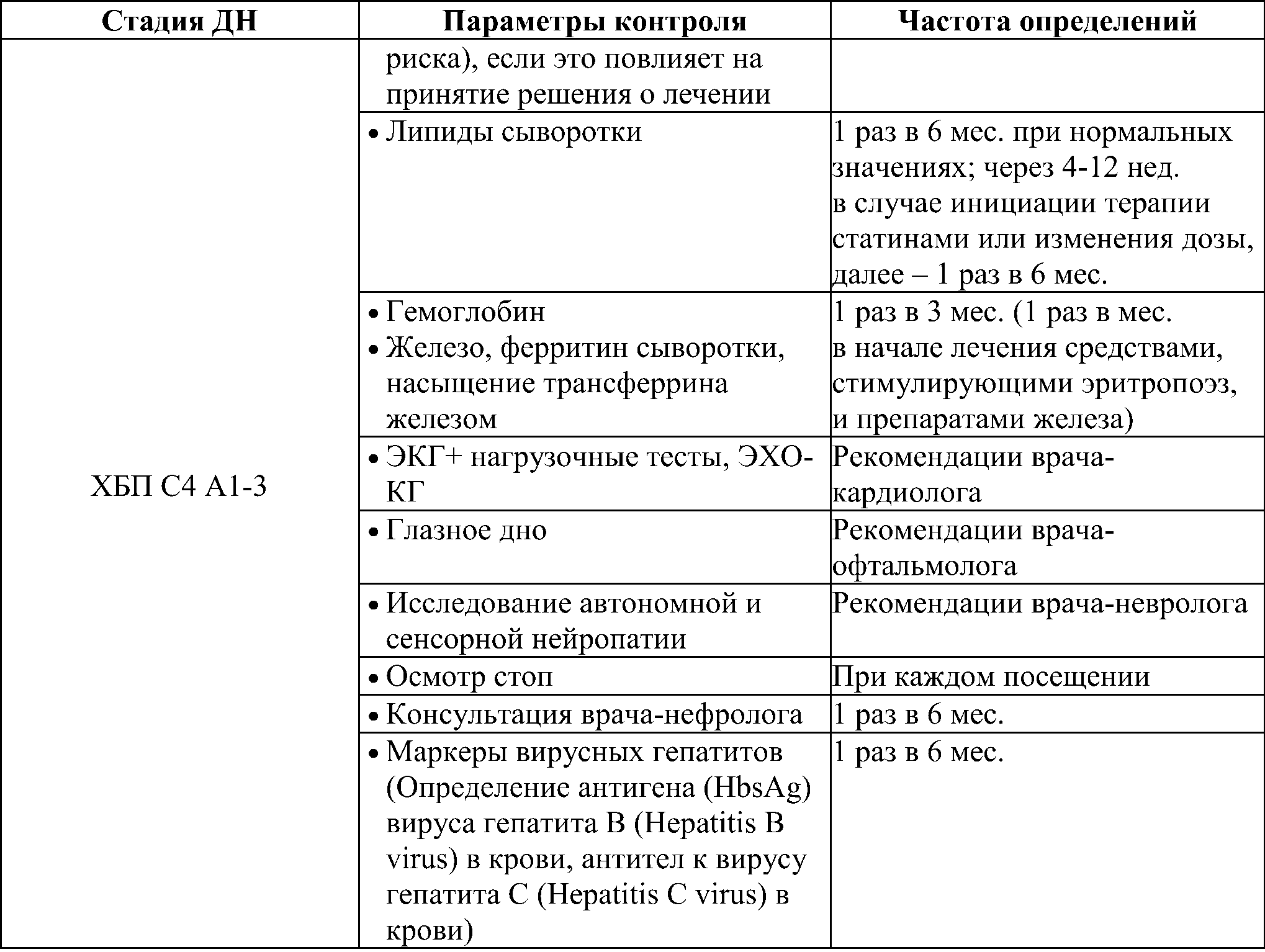
Диспансерное наблюдение включает мониторинг в зависимости от стадии ДН (табл. 22).
Таблица 22. Мониторинг в зависимости от стадии диабетической нефропатии
7.3 Диабетическая ретинопатия При СД поражение сетчатки проявляется виде диабетической ретинопатии (ДР) и/или диабетического макулярного отека (ДМО).
Подробные данные по ведению пациентов с сердечно-сосудистой патологией представлены в соответствующих клинических рекомендациях.
Диабетическая ретинопатия (ДР) — специфичное позднее нейромикрососудистое осложнение СД, развивающееся, как правило, последовательно от изменений, связанных с повышенной проницаемостью и окклюзией ретинальных сосудов до появления новообразованных сосудов и фиброглиальной ткани. Является одним из проявлений генерализованной микроангиопатии.
Диабетический макулярный отек (ДМО) — утолщение сетчатки, связанное с накоплением жидкости в межклеточном пространстве нейроэпителия вследствие нарушения гематоретинальных барьеров и несоответствия между транссудацией жидкости и способности к ее реабсорбции. ДМО может развиться при любой стадии ДР.
В основе патогенеза ДР лежит ишемия, развивающаяся из-за окклюзии капилляров сетчатки. Причиной нарушения перфузии сетчатки является поражение эндотелия сосудов
(эндотелиальный стресс) в условиях гипергликемии, приводящее к образованию тромбов в капиллярном русле.
Ишемия сетчатки приводит к повышению экспрессии сосудистого эндотелиального фактора роста VEGF (vascular endothelial growth factor).
Увеличение выработки VEGF выше критического уровня способствует развитию основных клинических проявлений диабетического поражения сетчатки – ДМО и неоваскуляризации [297, 298].
Частота развития ДР определяется длительностью СД.
Учитывая, что СД 2 может длительное время оставаться не диагностированным, ДР у пациентов с СД 2 часто выявляется на момент постановки диагноза.
По данным Федерального регистра СД в РФ на 01.01.2021 г. ДР регистрировалась у 13,5% пациентов с СД 2.
Классификация ДР, предложенная Kohner E. и Porta M. (1991), выделяет три основных стадии заболевания.
1. непролиферативная ДР;
2. препролиферативная ДР;
3. пролиферативная ДР.
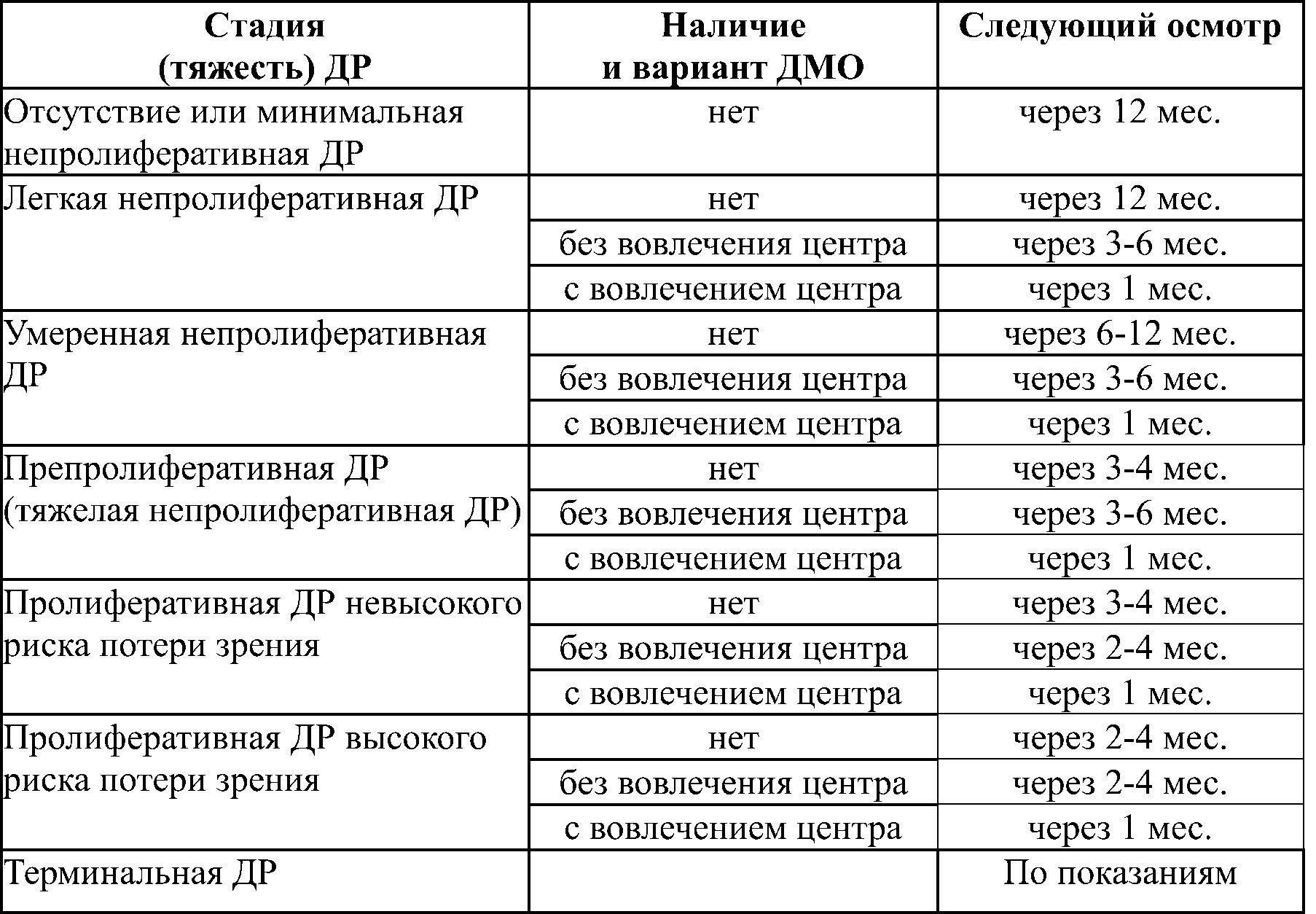
Клинические изменения, характерные для каждой стадии ДР, представлены в табл. 23.
Таблица 23. Характеристика изменений на глазном дне при различных стадиях диабетической ретинопатии
Самой полной на сегодняшний день является классификация Исследовательской группы по изучению раннего лечения ДР (Early Treatment Diabetic Retinopathy Study – ETDRS) 1991 года [346], которая также может быть использована в клинической практике (Приложение А3).
Диагностика
• Рекомендуется сбор анамнеза и жалоб при патологии глаза всем пациентам с СД 2 с подозрением на диабетическое поражение сетчатки с целью выяснения наличия функциональных зрительных расстройств .
Комментарии:
Возможно отсутствие жалоб в течение продолжительного времени, несмотря на прогрессирование заболевания.
Пациенты с ДР могут жаловаться на снижение остроты зрения, плавающие помутнения.
При ДМО пациенты отмечают искажения предметов (метаморфопсии), «пятно» перед взором, снижение остроты зрения.
При осложнениях пролиферативной ДР (преретинальных и интравитреальных кровоизлияниях) пациенты могут жаловаться на снижение зрения, «пятно», «сетку» перед глазами, при отслойке сетчатки — на снижение зрения и появление «завесы» в поле зрения.
Жалобы на снижение остроты зрения требуют, как правило, незамедлительного специализированного лечения.
При развитии нейропатии с поражением III и VI пар черепно-мозговых нервов пациенты могут жаловаться на отклонение глазного яблока, двоение и опущение верхнего века.
Из общего анамнеза важно уточнить давность СД и степень контроля заболевания (уровень глюкозы крови, гликированного гемоглобина), наличие артериальной гипертензии, показатели липидного обмена, наличие макрососудистых или иных микрососудистых осложнений СД.
• Рекомендуются осмотры врачом-офтальмологом всех пациентов c СД 2 при постановке диагноза СД, далее не реже 1 раза в год, с целью выявления диабетических изменений сетчатки.
Комментарии:
В связи с особенностью заболевания, отсутствием острого начала, СД 2 типа в течение нескольких лет может оставаться недиагностированным, что значительно увеличивает риск ДР.
Около 20% пациентов с СД 2 имеют признаки ДР в момент постановки диагноза СД.
В связи с этим пациенты должны быть полноценно осмотрены врачом-офтальмологом сразу в момент постановки диагноза СД 2.
Направление пациентов на обследование осуществляет врач-эндокринолог.
Объем диагностических процедур определяет врач-офтальмолог (см. соответствующие клинические рекомендации).
Как минимум должна быть проведена биомикроскопия глазного дна в условиях мидриаза.
Регулярные ежегодные осмотры всех пациентов с СД 2 имеют принципиально важное значение для своевременной идентификации лиц с риском развития тяжелой ДР, предотвращения ее прогрессирования и утраты зрения. Возможно отсутствие жалоб в течение продолжительного времени, даже при наличии пролиферативной ДР и ДМО.
Лечение
• Рекомендуется достижение целевых уровней гликемического контроля, АД и показателей липидного обмена у пациентов с СД 2 с целью предотвращения развития и прогрессирования ДР.
Комментарии: Для достижения этой цели следует осуществлять междисциплинарное ведение пациентов.
• Не рекомендуется консервативное лечение пациентов с СД 2 с ДР и/или ДМО.
Комментарии: Применение ангиопротекторов, антиоксидантов, ферментных препаратов и витаминов для лечения ДР у пациентов с СД 2 не имеет убедительной доказательной базы.
• Рекомендуется проведение всех необходимых лечебных офтальмологических манипуляций пациентам с СД 2 на любой стадии ДР и при ДМО для предотвращения потери зрения вне зависимости от достижения целевых уровней гликемического контроля, АД и липидного обмена .
• Рекомендуется проведение панретинальной лазерной коагуляции сетчатки (ЛКС) в условиях медикаментозного мидриаза пациентам с СД 2 на стадии препролиферативной ДР (относительное показание) в случае невозможности регулярного мониторинга с целью подавления экспрессии VEGF и профилактики развития неоваскуляризации, стабилизации или повышения корригированной остроты зрения.
Комментарии: Стандартная панретинальная ЛКС обычно осуществляется за несколько сеансов. Сеансы панретинальной ЛКС могут проводиться как в стационарных, так и в амбулаторных условиях при максимальном медикаментозном мидриазе.
• Рекомендуется проведение панретинальной ЛКС в условиях медикаментозного мидриаза, возможно, в сочетании с интравитреальным введением средства, препятствующего новообразованию сосудов (ранибизумаба**), пациентам с СД 2 на стадии пролиферативной ДР с целью подавления неоваскуляризации, стабилизации или повышения корригированной остроты зрения.
Комментарии: При наличии показаний к проведению панретинальной ЛКС, она должна выполняться вне зависимости от уровня НbA1c и не дожидаясь существенного улучшения гликемического контроля.
• Рекомендуется проведение фокальной ЛКС в условиях медикаментозного мидриаза, в том числе в сочетании с интравитреальными введениями средств, препятствующих новообразованию сосудов, или глюкокортикостероидов для местного применения пациентам с СД 2 при наличии клинически значимого ДМО с целью стабилизации или повышения корригированной остроты зрения.
• Рекомендуются интравитреальные инъекции (в условиях операционной) средств, препятствующих новообразованию сосудов – препаратов ранибизумаб** [234, 371] или глюкокортикостероидов (дексаметазон** в виде имплантата для интравитреального введения) [372], возможно в сочетании с ЛКС [370] пациентам с СД 2 при наличии клинически значимого ДМО с целью уменьшения толщины сетчатки, стабилизации или повышения корригированной остроты зрения.
Комментарии: В настоящее время интравитреальное введение средств, препятствующих новообразованию сосудов (ингибиторов ангиогенеза), является терапией первой линии при ДМО с вовлечением центра макулы. Необходимо учитывать, что при сочетании ЛКС и интравитреальных введений ингибиторов ангиогенеза, функциональный эффект отсроченного лазерного лечения будет лучше. В каждом клиническом случае окончательное решение о показаниях к лечению средствами, препятствующими новообразованию сосудов (ингибиторами ангиогенеза), выборе режима инъекций принимает врач-офтальмолог на основе оценки особенностей клинической картины и течения заболевания.
• Рекомендуется микроинвазивная витреоэктомия или витреошвартэктомия (в условиях операционной и медикаментозного мидриаза, при необходимости с сопутствующими манипуляциями, включая тампонаду витреальной полости (перфторорганическим или иным высокомолекулярным соединением), эндовитреальную замену перфторорганического соединения на силикон, эндовитреальное введение воздуха, силикона, эндолазеркоагуляцию, круговое или локальное эписклеральное пломбирование пациентам с СД 2 с пролиферативной ДР, осложненной организовавшимся гемофтальмом и/или тракционной отслойкой сетчатки с захватом области макулы и/или тракционно-регматогенной отслойкой сетчаткой и/или тракцией области макулы, а также при тракционном ДМО с целью восстановления нормальных анатомических соотношений, стабилизации или повышения корригированной остроты зрения.
Профилактика и диспансерное наблюдение • Рекомендуется устранение модифицируемых факторов риска возникновения и прогрессирования ДР и ДМО – достижение целевых уровней гликемического контроля, АД и показателей липидного обмена у пациентов с СД 2 с целью профилактики диабетических поражений глаз.
Комментарии: Целевые уровни представлены в разделе 3.1 Терапевтические цели.
• Рекомендуются регулярные офтальмологические осмотры с обязательной офтальмоскопией/биомикроскопией глазного дна всем пациентам с СД 2, частота которых зависит от особенностей клинической картины и течения заболевания, с целью выявления, оценки тяжести диабетических изменений сетчатки, их мониторинга и выработки тактики ведения пациента.
Комментарии: Частота офтальмологических осмотров пациентов с СД 2 представлена в табл. 24.
Таблица 24. Частота офтальмологических осмотров пациентов с сахарным диабетом 2 типа
Комментарии: При планировании периодичности осмотра врачом-офтальмологом следует учитывать, что риск развития и прогрессирования ДР и ДМО возрастает при определенных состояниях пациента, сопряженных с нарушениями гормонального статуса (беременность, состояние после искусственного прерывания беременности и другие).
При неожиданном снижении остроты зрения или появлении каких-либо жалоб со стороны органа зрения, обследование у врача-офтальмолога должно быть проведено по возможности скорее, вне зависимости от сроков очередного визита к врачу.
7.4 Диабетическая нейропатия
Диабетическая нейропатия (ДНП) – комплекс клинических и субклинических синдромов, каждый из которых характеризуется диффузным или очаговым поражением периферических и/или автономных нервных волокон в результате СД.
Сенсо-моторная нейропатия – поражение соматической нервной системы, сопровождающееся снижением различных видов чувствительности, атрофией межкостных мышц, ригидностью суставов и характерной деформацией стопы.
Автономная нейропатия – поражение симпатического и парасимпатического отдела периферической нервной системы.
Основными патогенетическими механизмами ДНП признаны активизация полиолового пути метаболизма глюкозы, ангиопатия vasa nervorum, оксидативный стресс, дефицит миоинозитола, а также недостаточность оксида азота.
При СД 2 значима роль и нарушений липидного обмена.
Все это ведет к снижению скорости проведения возбуждения по нервному волокну.
Согласно данным эпидемиологических исследований, распространенность ДНП при НТГ составляет 10-13%, а при явном СД 2 — 35-55% .
Классификация диабетической нейропатии. 1. Дистальная симметричная полинейропатия:
> С преимущественным поражением тонких нервных волокон
> С преимущественным поражением толстых нервных волокон
> Смешанная (наиболее распространенная)
2. Автономная нейропатия:
— Кардиоваскулярная:
> Снижение вариабельности сердечного ритма
> Тахикардия покоя
> Ортостатическая гипотензия
> Внезапная смерть (злокачественная аритмия)
— Гастроинтестинальная:
> Диабетический гастропарез (гастропатия)
>Диабетическая энтеропатия (диарея)
> Снижение моторики толстого кишечника (констипация)
— Урогенитальная:
> Диабетическая цистопатия (нейрогенный мочевой пузырь)
> Эректильная дисфункция
> Женская сексуальная дисфункция
— Судомоторная дисфункция:
> Дистальный гипогидроз/ангидроз
— Нарушение распознавания гипогликемий
Б. Мононейропатия (мононевриты различной локализации) (атипичные формы):
1. Изолированные поражения черепно-мозговых или периферических нервов
2. Мононевриты различной локализации (в том случае, если полинейропатия исключена)
В. Радикулопатия или полирадикулопатия (атипичные формы):
1. Радикулоплексопатия (пояснично-крестцовая полирадикулопатия,
проксимальная моторная амиелотрофия)
2. Грудная радикулопатия
Г. Недиабетические нейропатии, сопутствующие СД:
1. Туннельные синдромы
2. Хроническая воспалительная демиелинизирующая полинейропатия
3. Радикулоплексопатия
4. Острая болевая нейропатия с поражением тонких нервных волокон
Комментарии:
В современной медицинской литературе и в рекомендациях по диагностике и лечению поражений нервной системы у пациентов с СД, предлагаемых различными медицинскими сообществами, нет единой классификации ДНП. Термин «диффузная», использованный в приведенной выше классификации, отражает, в первую очередь, выраженность и распространенность поражения нервного волокна.
Согласно современным данным связь автономной нейропатии и нераспознавания гипогликемий не является очевидной.
Стадии нейропатии
I. Доклиническая
II. Клинических проявлений
III. Осложнений
Для подавляющего числа пациентов с СД 2 и ДНП характерны жалобы на боли в нижних конечностях (боли в стопах различной интенсивности в покое, чаще в ночные и вечерние часы, онемение, парестезии, зябкость стоп, судороги в мышцах голеней и стоп парестезии, жжение в стопах), сухость кожи, атрофия мышц, характерная деформация пальцев (молоткообразная деформация).
Комментарии: Необходимо помнить, что клиническая картина большого числа других заболеваний имеет сходные жалобы, неспецифические для ДНП. Таким образом, при сборе анамнеза необходимо обратить внимание на наличие сопутствующих, непосредственно не связанных с СД заболеваний, которые могут участвовать в патогенезе возникновения болевого синдрома в нижних конечностях (артрозы, венозная недостаточность, радикулопатии и т.п.). Всем пациентам с СД 2 и трофическими язвами стоп необходимо провести оценку болезненности язвенных дефектов для выявления нейропатических ран. Необходимо помнить, что перенесенные ранее травмы, оперативные вмешательства на нижних конечностях, острое нарушение мозгового кровообращения, сопровождающиеся различной степенью выраженности поражением нервной проводимости в нижних конечностях, могут приводить к одностороннему изменению чувствительности. Следует придерживаться общих принципов лечения любых нейропатических язв у пациентов с СД.
Диагностика
• Рекомендуется проводить оценку клинических признаков нейропатии (жалоб, состояния периферической чувствительности и сухожильных рефлексов) у всех пациентов с СД 2 при постановке диагноза СД, далее не реже 1 раза в год, для диагностики ДНП.
Комментарии: Для диагностики ДНП можно использовать диагностические шкалы, например:
шкала симптомов нейропатии (Neuropathy Symptom Score, NSS) [390–393]. Сумма баллов >5 говорит о наличии выраженной нейропатии (Приложение Г2);
Мичиганский опросник для скрининга нейропатии (The Michigan Neuropath Screening Instrument, MNSI) [394–397]. Сумма баллов >2 позволяет подозревать наличие нейропатии
(Приложение Г3);
опросник DN4 для диагностики болевой нейропатии [398, 399]. Сумма баллов >4 свидетельствует о нейропатическом характере боли (Приложение Г4).
• Рекомендуется проводить исследование чувствительности периферической нервной системы у всех пациентов с СД 2 при постановке диагноза СД, далее не реже 1 раза в год, для выявления ДПН .
Комментарии: Для диагностики ДНП достаточно тщательно собранного анамнеза, определения порога температурной (или тактильной) чувствительности, а также вибрационной чувствительности с помощью градуированного камертона 128 Гц. В настоящее время не существует достоверных лабораторных исследований для подтверждения наличия ДНП.
• Рекомендуется проводить исследование с помощью монофиламента 10 г всем пациентам с СД 2 для определения риска формирования трофических язв стоп и ампутации.
Комментарии: Достоверность полученных результатов повышается при дополнительной оценке других видов чувствительности (вибрационной с помощью градуированного камертона 128 Гц, болевой, температурной) и/или сухожильных рефлексов.
• Рекомендуется выявлять возможные симптомы и признаки автономной нейропатии у пациентов с СД 2 и диабетическими микроангиопатиями для обеспечения надлежащей терапии.
• Рекомендуется проведение электроннейромиографии периферических нервов пациентам с СД 2 при неэффективности стандартной терапии ДНП в течение 6 месяцев для выявления редко встречающихся форм поражения периферических нервов при СД или сопутствующей неврологической патологии.
Комментарии: Проведение электронейромиографии периферических нервов у пациента с хроническим раневым дефектом стопы нецелесообразно, так как значительно усложняет обследование, а ее результат не влияет на выработку плана лечебных мероприятий.
Лечение
• Рекомендуется достижение и поддержание индивидуальных целевых показателей углеводного обмена у пациентов с СД 2 для успешного лечения ДНП.
Комментарии: Оптимизация гликемического контроля позволяет предотвратить или отсрочить развитие ДНП у пациентов с СД 2.
• Рекомендуется применение медикаментозной терапии пациентам с СД 2 с болевой формой ДНП для купирования ее симптомов.
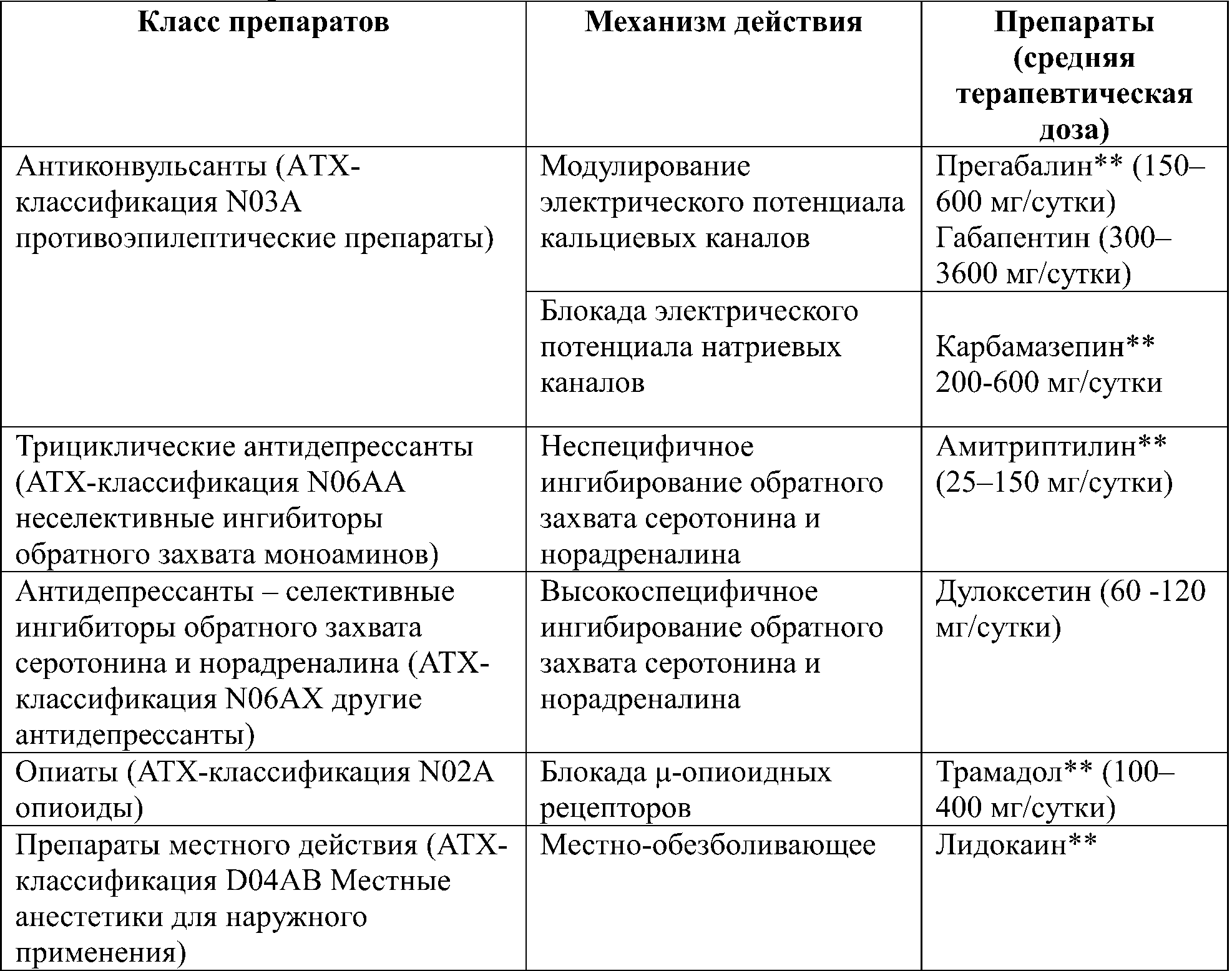
Комментарии: Препараты, применяемые для лечения болевой формы дистальной полинейропатии перечислены в табл. 25.
Таблица 25. Препараты, применяемые для лечения болевой формы диабетической нейропатии
Реабилитация
• Рекомендуется достижение и поддержание индивидуальных целевых показателей углеводного обмена, применение обезболивающей терапии с учетом психосоматического состояния, уход за ногами пациентам с СД 2 и болевой ДНП для предотвращения прогрессирования осложнения и минимизации риска развития трофических язв.
Профилактика и диспансерное наблюдение
Единственным на сегодняшний день методом профилактики прогрессирования ДНП является достижение и поддержание индивидуальных целевых показателей углеводного и липидного обмена. Оценку состояния периферической чувствительности необходимо проводить не реже 1 раза в год. Наличие сопутствующих заболеваний центральной нервной системы и периферических нервов различного генеза, заболеваний периферических артерий может ускорить прогрессирование ДНП и ухудшить клинический прогноз.
7.5 Диабетическая остеоартропатия Диабетическая остеоартропатия (ДОАП), нейроартропатия или стопа Шарко -безболевая, прогрессирующая деструкция одного или нескольких суставов стопы на фоне ДНП.
В результате демиелинизации моторных волокон развивается слабость связочного аппарата стоп, приводящая к нестабильности суставов.
Автономная нейропатия приводит к денервации сосудистой стенки и, как следствие, развитию артерио-венозных шунтов и, как следствие, усилению кровотока, что ведет к активации резорбции костной ткани и остеопении.
Кость теряет не только плотность, но и эластичность, что делает скелет стопы менее устойчивым к травмам.
Как правило, пусковым фактором ДОАП является мелкая, не замеченная пациентом механическая травма.
Незначительное по силе внешнее воздействие приводит к переломам костей, подвывихам и вывихам суставов.
Ситуация усугубляется отсутствием протективной болевой чувствительности.
Пациент продолжает опираться на поврежденную конечность, что приводит к вовлечению в процесс новых костей и суставов.
Развивается остеохондральная фрагментация и выраженная дегенерация суставов.
В тяжелых случаях стопа может полностью утратить опорную функцию, что может потребовать проведения ампутации.
Доказано, что пациенты с ДНП имеют большую частоту развития костно-суставных изменений, чем лица без неврологических нарушений.
Различные исследования ДОАП выявили высокую частоту ее развития у пациентов с длительностью СД более 12 лет, независимо от возраста и пола.
У большинства обследованных процесс односторонний, тогда как двустороннее поражение встречается лишь в 9-25% случаев.
Как правило, это лица с длительной декомпенсацией СД, независимо от его типа и методов лечения. Отмечено, что у 73% пациентов предшествующие деформации, травмы не регистрировались.
В клинической картине ДОАП выделяют острую и хроническую стадии. Острая стадия характеризуется преобладанием воспалительных процессов в ответ на имеющееся повреждение.
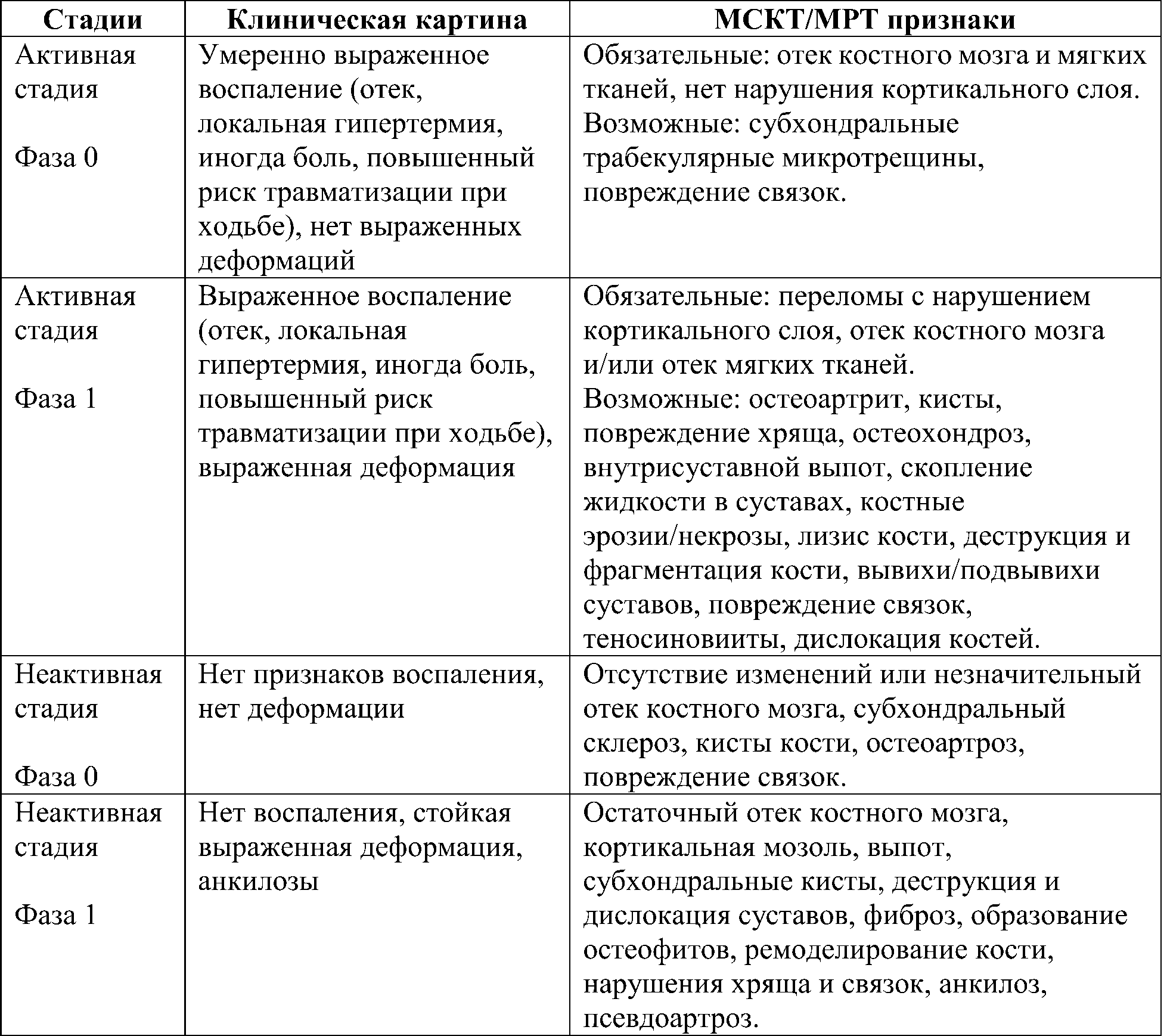
Классификация ДОАП приведена в табл. 26.
Таблица 26. Классификация диабетической остеоартропатии на основании клинической картины, МРТ/МСКТ признаков [412]
Диагностика
• Рекомендуется проведение клинического (осмотр, пальпация) и инструментального (инфракрасная термометрия, оценка периферической чувствительности, МРТ, рентгенография, МСКТ) обследования пациентам с СД 2 для диагностики ДОАП.
Комментарии: Диагноз ДОАПустанавливается на основании характерных данных анамнеза, жалоб и клинической картины (гипертермия, деформация, отек пораженной конечности), результатов инструментальных и лабораторных методов исследования. В типичных случаях диагноз не вызывает затруднений. Специфичных для остеоартропатии маркеров костного метаболизма и тестов лабораторной диагностики в настоящее время нет. Основным методом инструментальной диагностики и дифференциальной диагностики ДОАП остается рентгенография. При этом на рентгенограмме отражаются гипертрофические, либо атрофические изменения, возникающие в ответ на повреждение. В типичных случаях для постановки диагноза в хронической стадии ДОАП не требуется других дополнительных инструментальных методов обследования.
• Рекомендуется проводить инфракрасную термометрию кожи пораженной и не пораженной конечности всем пациентам с СД 2 с подозрением на острую стадию ДОАП для диагностики данного осложнения.
• Рекомендуется проведение МРТ стопы и голеностопного сустава пациентам с СД 2 для верификации острой стадии ДОАП .
Комментарии:
Основные сложности возникают при диагностике острой стадии осложнения, когда, при наличии типичной клинической картины, рентгенографические изменения отсутствуют, а также при проведении дифференциального диагноза ДОАП и остеомиелита.
В этой связи следует обратить особое внимание на то, что отсутствие изменений на рентгенограмме при наличии клинической картины (отек, гипертермия, деформация стопы) не означает отсутствия ДОАП. Несоответствие клинической и рентгенологической картин наблюдается на ранних стадиях развития осложнения достаточно часто («предварительная стадия», «стадия 0»). В такой ситуации тщательно собранный анамнез, клинический осмотр с проведением неврологических тестов и МРТ помогут с большой долей вероятности поставить диагноз ДОАП.
• Рекомендуется проведение МРТ пораженной стопы и голеностопного сустава пациентам с СД 2 для дифференциальной диагностики ДОАП и остеомиелита.
• Рекомендуется проведение фистулографии, МСКТ стопы и голеностопного сустава для дифференциальной диагностики острой стадии ДОАП и остеомиелита у пациентов с хронической раной стопы и н/3 голени.
Комментарии: При наличии ДОАП с плантарной язвой необходимо провести дифференциальный диагноз между острой стадией ДОАП и остеомиелитом. Это имеет ключевое значение для назначения адекватной антибактериальной терапии и выбора тактики хирургической коррекции.
Сочетание позитронно-эмиссионной томографии и компьютерной томографии (ПЭТ/КТ) позволяет с высокой точностью обнаружить локализацию патологических изменений на самых ранних стадиях, проследить за стадиями развития и количественно оценить метаболическую активность процесса, для контроля прогрессирования осложнения.
Лечение
• Рекомендуется разгрузка пораженной конечности с помощью индивидуальной разгрузочной повязки (ИРП) или ортеза у всех пациентов с СД 2 с острой стадией ДОАП для предотвращения прогрессирования деструктивных процессов в костносуставном аппарате стопы.
Комментарии: Комплекс лечебных мероприятий при ДОАП определяется стадией осложнения. Основной целью лечения в острой стадии процесса является, предотвращение развития дальнейшей деформации и травматизации стопы. Для достижения поставленной цели применяются методы максимальной разгрузки пораженной конечности – наложение ИРП или использование ортопедического аппарата (ортеза). Иммобилизацию конечности необходимо начинать как можно раньше. При наличии клинической картины, соответствующей острой стадии ДОАП (отек, гипертермия стопы) и отсутствии инструментального подтверждения (рентгеннегативная стадия, невозможность проведения МРТ) лечебная тактика должна быть такой же, как при установленном диагнозе ДОАП. Относительным противопоказанием для наложения несъемного варианта ИРП при ДОАП является наличие язвенного дефекта, требующего ежедневного контроля и смены повязки. Абсолютным противопоказанием для наложения ИРП (как несъемного, так и съемного вариантов) является наличие обширного гнойнодеструктивного процесса, требующего обязательной хирургической обработки.
• Рекомендуется использовать ИРП в течение 4-8 мес. пациентам с СД 2 до перехода острой стадии ДОАП в хроническую для предотвращения возможной деформации сустава.
Комментарии: В настоящее время нет убедительных доказательств эффективности использования лекарственных препаратов для лечения ДОАП (бисфосфонаты, кальцитонин). Кроме того, бисфософонаты противопоказаны при нарушении функции почек, которое достаточно часто выявляется у пациентов с длительно текущим и плохо контролируемым СД.
• Рекомендуется постоянное ношение сложной ортопедической обуви пациентам с СД 2 с хронической стадией ДОАП для предотвращения травматизации стопы, новых переломов и образования плантарных язвенных дефектов.
Комментарии: Целью лечебно-профилактических мероприятий на стадии консолидации (хронической стадии) является предотвращение травматизации стопы, новых переломов и образования плантарных язвенных дефектов. На этой стадии нет необходимости в максимальной постоянной иммобилизации конечности. После снятия ИРП рекомендовано постепенное расширение двигательного режима. В качестве промежуточных методов фиксации и разгрузки стопы можно применять съемный ИРП не на целый день, а также использовать ортопедические аппараты. Принципиально важное значение в хронической стадии отведено выбору обуви. Требования к обуви зависят от типа поражения и сформировавшейся деформации стопы. Если деформация стопы минимальна, достаточно постоянного ношения профилактической обуви для пациентов с СД 2.
• Рекомедуется проведение консультации врача-травматолога-ортопеда пациентам с выраженной деформацией стопы или деформацией по типу «стопы-качалки» для решения вопроса об изготовление сложной ортопедической обуви.
• Рекомендуется консультация врача-травматолога-ортопеда пациентам с СД 2 с выраженной деформацией конечности вследствие ДОАП для решения вопроса о возможности выполнения оперативного корригирующего вмешательства.
Комментарии:
В последнее время все большее распространение приобретает реконструктивная хирургия ДОАП. Основным показанием к проведению оперативных вмешательств на стопе является неэффективность консервативных методов лечения, которая проявляется рецидивирующими плантарными язвенными дефектами и/или невозможностью сохранять стабильность стопы во время ходьбы. Оперативное вмешательство должно четко соответствовать поставленной задаче. Если преобладает нестабильность в области голеностопного или других суставов, применяется артродез с жесткой внутренней фиксацией. В случае рецидивирования язвенных дефектов выполняется экзостэктомия с последующей хирургической обработкой раны. Если язвенный дефект осложняется остеомиелитом, проводится антимикробная терапия, экзостэктомия, хирургическая обработка раны. Достаточно часто выявляется укорочение ахиллова сухожилия, которая ведет к дополнительной деформации стопы и увеличению нагрузочного давления на передний отдел стопы. Таким пациентам показано оперативное вмешательство по удлинению ахиллова сухожилия. Лечебная тактика в послеоперационном периоде полностью соответствует ведению пациента с острой стадией ДОАП: иммобилизация, включая изготовление ИРП, дозированное расширение двигательного режима после заживления.
• Рекомендуется проводить регулярные консультации врача-травматолога-ортопеда пациентов с СД 2 и с хронической стадией ДОАП для подбора индивидуального ортопедического пособия (готовая терапевтическая обувь, изготовление тутора или ортеза, изготовление индивидуальной ортопедической обуви).
Комментарии: Адекватность изготовленной ортопедической обуви должна регулярно оцениваться лечащим врачом (врачом-эндокринологом, хирургом, специалистом кабинета диабетической стопы) и меняться не реже 1 раза в год.
Профилактика и диспансерное наблюдение
Профилактика прогрессирования ДОАП включает в себя поддержание обучение правилам ухода за ногами, при необходимости профессиональный подиатрический уход, постоянное ношение готовой или индивидуальной ортопедической обуви, динамическое наблюдение у врача-эндокринолога и врача-травматолога-ортопеда по месту жительства.