1.5.1 Классификация временных периодов ишемического инсульта
1.5.2 Классификация патогенетических подтипов SSS-TOAST.
1.5.3. Классификация CASCADE
1.5.4 Источники высокого кардиоэмболического риска.
1.5.5 Лакунарный инсульт.
1.5.6 Диагностические критерии диссекции как потенциальной причины инсульта согласно классификации ASCOD
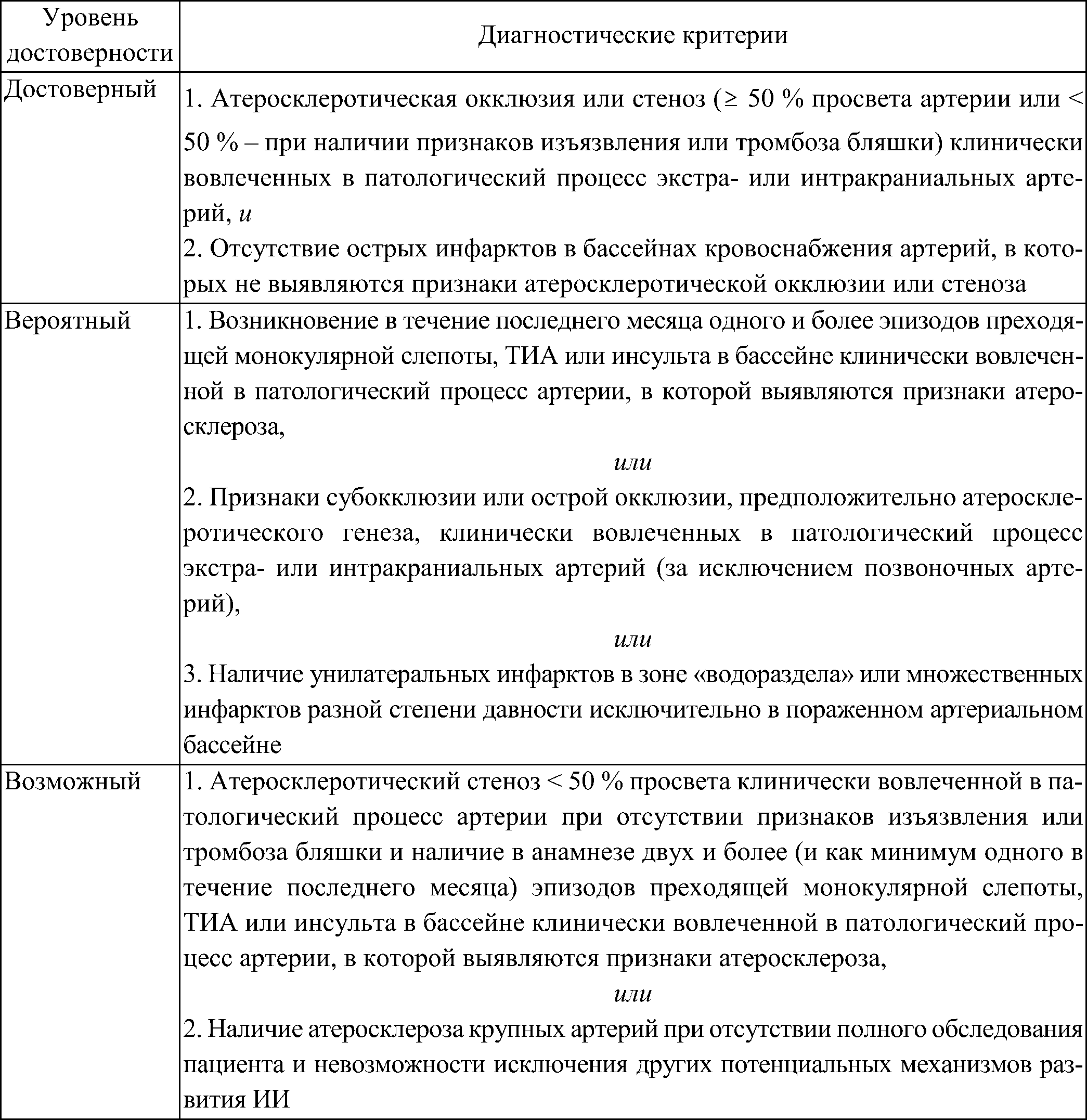
Таблица 1 Ишемический инсульт, обусловленный атеросклеротическим поражением крупных артерий (атеротромботический)
Таблица 2. Ишемический инсульт, обусловленный кардиогенной тромбоэмболией (кардиоэмболический)
Таблица 3. Ишемический инсульт, обусловленный окклюзией мелких артерий (лакунарный)
Таблица 4. Ишемический инсульт, обусловленный другой установленной этиологией
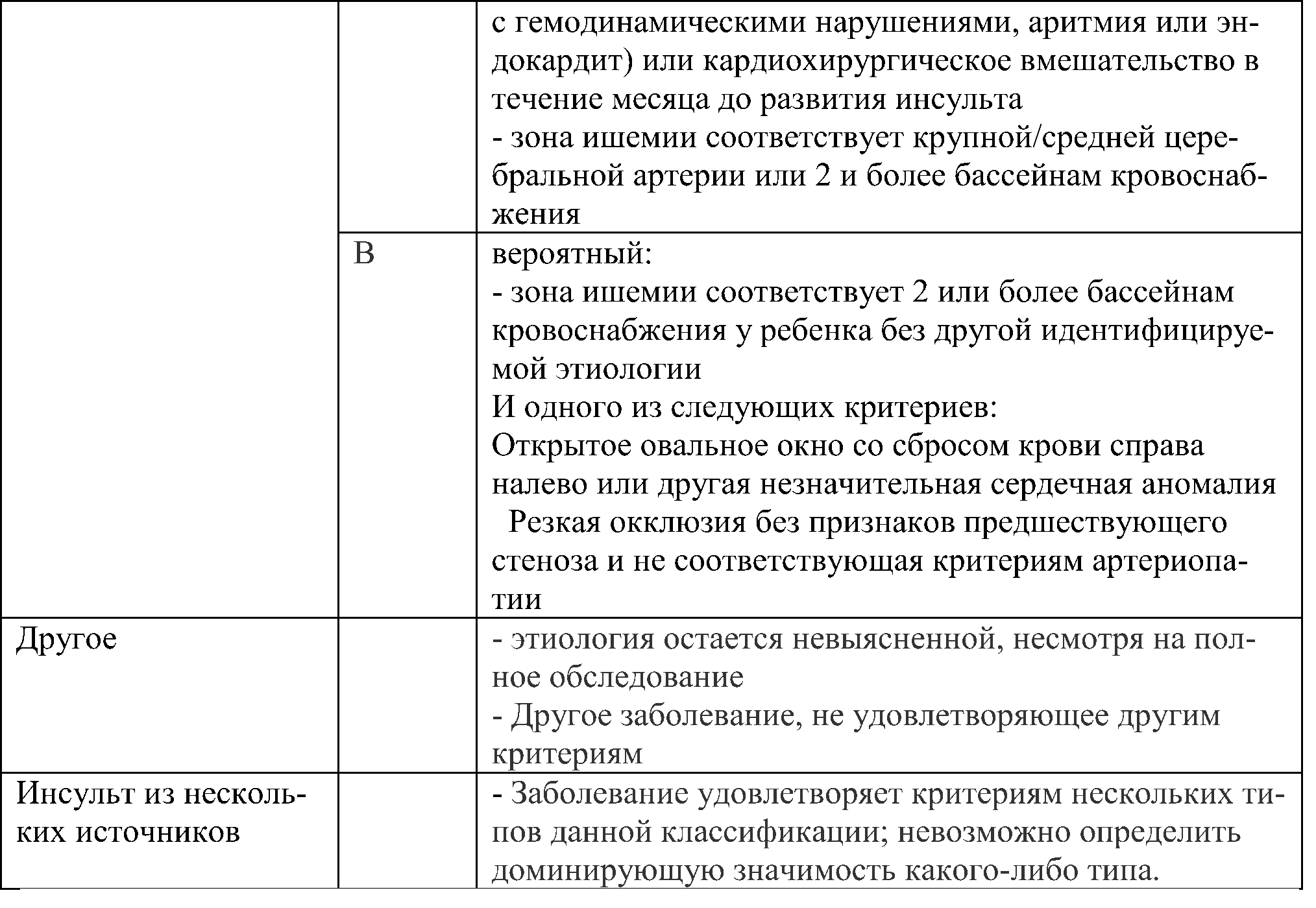
Таблица 4а. Стандартизированная классификация и диагностическая оценка артериального ишемического инсульта у детей.
1.5. Классификация заболевания или состояния (группы заболеваний или состояний)
Согласно классификации SSS-TOAST, автоматизированная версия которой называется Causative Classification System выделяют
Патогенитические подтипы ишемического инсульта:
По шкале ECST используют отношение диаметра сохраненного просвета артерии к предполагаемому истинному размеру (измерение проводят на уровне ампулы ВСА).
По шкале NASCET применяют отношение сохраненного просвета артерии в области ампулы к диаметру ВСА над областью стеноза в области, где стенки артерии становятся параллельными друг другу.
Степень стеноза 50% по шкале NASCET соответствует 75% по шкале ECST, 60% по шкале NASCET -80% по шкале ECST.
Приоритетной считают методику NASCET.
К основным механизмам развития инсульта относятся артерио-артериальная эмболия (пассаж тромба или фрагмента атеромы), гипоперфузия или их сочетание.
Клиническая картина атеротромботического инсульта неспецифична и зависит от конкретного патогенетического механизма, однако можно выделить несколько клинических подсказок:
ТИА в заинтересованном артериальном бассейне,
транзиторная ипсилатеральная моноокулярная слепота,
атеросклеротическое поражение других артериальных бассейнов (коронарные, периферические артерии),
локализация инфаркта мозга в смежных зонах кровообращения (особенно внутренних)
наличие старых инфарктов в том же сосудистом бассейне [50, 51] (табл. 1).
– ИИ вследствие артериальной окклюзии эмболом, предположительно сформированным в сердце [45].
В большинстве случаев кардиоэмболический инсульт развивается на фоне фибрилляции предсердий, при этом он часто характеризуется острым развитием неврологического дефицита и его максимальной выраженностью в дебюте заболевания.
Поражение проксимальных отделов мозговых артерий проявляется грубым неврологическим дефицитом, однако дистальное смещение эмбола может привести к быстрому регрессу симптомов. При визуализации могут выявляться инфаркты мозга (как острые, так и хронические) в нескольких артериальных бассейнах [52, 53].

Клиническая картина лакунарного инсульта неспецифична.
Лакунарные синдромы (гемигипестезия и гемипарез, изолированная гемигипестезия, изолированный гемипарез, синдром дизартрия – неловкая кисть и атактический гемипарез) нередко развиваются у пациентов с другими патогенетическими подтипами инсульта.
Большей специфичностью обладают синдромы изолированной гемигипестезии и атактического гемипареза.
Нечастым, но важным клиническим признаком лакунарного инсульта выступает синдром «предупреждающей внутренней капсулы» (capsular warning syndrome), который проявляется рецидивирующим транзиторным моторным или сенсомоторным лакунарным синдром с вовлечением двух из трех частей тела (лицо, рука, нога) и полным восстановлением между эпизодами.
Более чем у трети пациентов с лакунарным синдромом наблюдается нарастание неврологического дефицита в первые дни заболевания.
Основой верификации лакунарного инсульта является визуализация инфаркта размером менее 20 мм в бассейне перфорантной артерии (глубинные отделы больших полушарий, мост).
При наличии инфаркта менее 20 мм в корково-субкортикальной зоне лакунарный подтип инсульта неправомочен.
Если лакунарный инсульт развивается на фоне выраженной церебральной микроангиопатии, то в клинической картине помимо очагового неврологического дефицита могут наблюдаться сосудистые когнитивные нарушения, постуральные и тазовые расстройства.

Другими причинами ИИ служат:
невоспалительные артериопатии (диссекция; фибромышечная дисплазия, в частности каротидная сеть (carotid web); синдром обратимой церебральной вазоконстрикции; болезнь мойя-мойя; болезнь Фабри; CADASIL и др.),
воспалительные артериопатии (первичный ангиит центральной нервной системы; гигантоклеточный артериит; васкулит на фоне диффузных заболеваний соединительной ткани; инфекционный васкулит на фоне сифилиса, туберкулеза, других бактериальных инфекций, varicella-zoster, ВИЧ и др.);
токсическая артериопатия;
мигрень-ассоциированный инсульт;
MELAS и гематологические заболевания (наследственные тромбофилии, антифосфо-липидный синдром, серповидноклеточная анемия, истинная полицитемия, эссециальный тромбоцитоз и др.)

Развитию диссекции обычно предшествует механический триггер, а в клинической картине наблюдается цефалгия и/или цервикалгия на стороне поврежденной артерии.
Важной клинической подсказкой в отношении диссекции внутренней сонной артерии выступает синдром Горнера или периферический парез языка.
(А (атеросклероз), S (болезнь мелких сосудов), C (кардиальная патология), O (другая причина) и D (диссекция)):
свидетельство развития гематомы по данным одного из исследований – Т1 FS МРТ, TOF-MРA, КТ (аксиальные срезы),
аутопсия – утолщение артериальной стенки за счет гематомы с сужением просвета;
или УЗИ (гипоэхогенная артериальная стенка с сужением просвета и резким увеличение диаметра сонной или позвоночной (V2) артерии).
применение менее чувствительного или менее специфического диагностического теста (только протяженный артериальный стеноз дистальнее бифуркации сонной артерии или в V2, V3 или V4 сегменте позвоночной артерии без признаков гематомы артериальной стенки по данным селективной ангиографии и/или УЗИ, и/или КТА, и/или МРА) или соответствие результатов УЗИ реканализации в течение периода наблюдения [64].
Эмболический инсульт из неустановленного источника эмболии (ESUS, embolic stroke of undetermined source) — инсульт, имеющий нелакунарный паттерн при нейровизуализации, без очевидных источников эмболии после проведения дообследования и исключения известных причин инсульта, в частности источников кардиоэмболии и атеросклероза проксимально зоне инсульта.
1. пароксизмальная форма фибрилляции предсердий,
2. предсердная кардиомиопатия (не связанная с фибрилляцией предсердий),
3. эмбологенные атеросклеротические бляшки с сужением просвета артерии менее 50 %,
4. атерома дуги аорты и открытое овальное окно.
Нередко встречается ситуация, когда у пациента имеются две и более потенциальных причины инсульта, например фибрилляция предсердий и ипсилатеральный стеноз внутренней сонной артерии более 50 %.
Также может случиться, что имеют место причины, выраженность каждой из которых недостаточна для того, чтобы объяснить инсульт, например ипсилатеральный стеноз внутренней сонной артерии от 30 до 50 % и апикальная акинезия левого желудочка.
В данных ситуациях целесообразно использование фенотипической классификации ASCOD.
Временные периоды ИИ у детей соответствуют таковым во взрослой популяции.
По данным первых исследований классифицировать этиологию детского инсульта по критериям взрослой популяции невозможно вследствие несоответствия критериям атеросклеротического, кардиоэмболического и ИИ, обусловленного эмболией мелких сосудов [66].